微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 设nA为阿伏伽德罗常数的数值,下列说法正确的是(????)
A.标准状况下,2.24L苯含有的分子数为0.1nA
B.25℃时,pH=13的Ba(OH)2溶液中含有OH-的数目为0.2nA
C.1 L 0.1 mol・L-1 Al2(SO4)3溶液中Al3+的数目为0.2nA
D.1.5molNO2与足量H2O反应,转移的电子数为nA
参考答案:D
本题解析:
试题分析:标况下苯是液体,不能用摩尔体积进行计算,A错误;B项的氢氧化钡溶液没有给出体积,不可以计算其中的OH-数目,B错误;C项中的硫酸铝溶液发生水解,氯离子数目不可计算,C错误;D正确;故选D。
本题难度:一般
2、选择题 设NA表示阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下,11.2 L乙醇中含有的碳氢键数为2.5NA
B.常温常压下,28 g C2H4、CO的混合气体中含有碳原子的数目为1.5NA
C.常温下,20 L pH=12的Na2CO3溶液中含有的OH-离子数为0.2NA
D.标准状况下,2.24 L Cl2与足量的NaOH溶液反应,转移的电子数目为0.2NA
参考答案:C
本题解析:
试题分析:A. 标准状况下乙醇是液态,无法计算,错误;B. 常温常压下,28 g C2H4、CO的混合气体中含有碳原子的数目为在NA和1.5NA之间,错误;C.常温下,20 L pH=12的Na2CO3溶液中含有的OH-离子数为0.2NA,正确;D. 标准状况下,2.24 L Cl2与足量的NaOH溶液反应,转移的电子数目应为0.1NA,错误;A的运用。
本题难度:一般
3、选择题 将30 mL 0.5mol/LNaOH溶液加水稀释到50 0 mL,稀释后NaOH的物质的量浓度为(??)
0 mL,稀释后NaOH的物质的量浓度为(??)
A.0.3 mol/L
B.0.03 mol/L
C.0.05 mol/L
D.0.04 mol/L
参考答案:B
本题解析:略
本题难度:一般
4、选择题 10 g 10%的氢氧化钠溶液稀释成50 mL,所得氢氧化钠溶液的物质的量浓度为
A、0.02 mol/L B、0.05 mol/L
C、0.25 mol/L D、0.5 mol/L
参考答案:D
本题解析:
正确答案:D
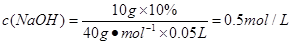
本题难度:一般
5、填空题 (12分)
(1)实验室用氯化铵固体制取氨气的化学方程式是 。
(2)将4.48L(标准状况)氨气通入水中得到0.05L溶液,所得溶液的物质的量浓度是 。
(3)现有100mL AlCl3与MgSO4的混合溶液,分成两等份。
①向其中一份中加入10mL 4mol/L的氨水,恰好完全反应,其中AlCl3与氨水反应的离子方程式是 。继续加入l mol/L NaOH溶液至10mL时,沉淀不再减少,沉淀减少的离子方程式是 ,减少的沉淀的物质的量是 。
②向另一份中加入a mL 1mol/LBaCl2溶液能使SO42-沉淀完全,a= 。
参考答案:(1)Ca(OH)2+2NH4Cl 本题解析:
本题解析:
(1)实验室用氯化铵固体制取氨气的化学方程式是Ca(OH)2+2NH4Cl CaCl2+2H2O+2NH3↑
CaCl2+2H2O+2NH3↑
(2)c(NH3)="(4.48L/22.4L" ・mol-1)/0.05L="4" mol/L
(3)①A13++3NH3・H2O=Al(OH)3↓+3NH4+
Al(OH)3+OH-=AlO2-+2H2O
减少的沉淀的物质的量
N(NaOH )=" l" mol/L×0.010L="0.01" mol
Al(OH)3+OH-=AlO2-+2H2O
0.01 mol 0.01 mol
故减少的沉淀的物质的量是0.01 mol
②n(MgSO4)=(0.010L×4mol/L
本题难度:一般