微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 已知A―O分别代表一种物质,它们之间的转化关系如下图所示(反应条件略)。A、B、H分别是由短周期元素组成的单质。B与冷水缓慢反应,与沸水迅速反应,放出氢气。D是一种离子化合物,其阴阳离子的个数比为2:3,且能与水反就应得到两种碱。C为淡黄色固体化合物,O能与G的水溶液反应生成蓝色沉淀。请回答下列问题:
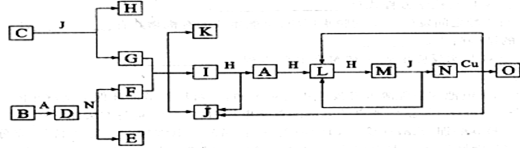
⑴组成B单质的元素位于周期表位置________________。化合物C电子式为____________。
⑵J的沸点比硒化氢(H2Se)的熔沸点高,其原因是_________________。
⑶I与H在一定条件下也可直接反应生成L和J, 写出化学方程式:_______________。
⑷写出D与水反应的化学方程式:_____________________。
⑸红棕色污染气体M的处理具有实际意义。现在常利用反应
M + NH3 N2+H2O(方程没配平)来处理M。当转移0.4mol电子时,消耗的M在标准状况下是???????L。
N2+H2O(方程没配平)来处理M。当转移0.4mol电子时,消耗的M在标准状况下是???????L。
2、选择题 1941年才第一次制得卤素的第五个成员――砹(At)。下列关于砹及其化合物的性质的预测中,不正确的是( )。
A.砹与碱金属单质钠能发生反应生成NaAt
B.卤素阴离子的还原性强弱次序是:F->Cl->Br->I->At-
C.砹的最高价氧化物对应水化物(HAtO4)的酸性比高碘酸(HIO4)的酸性弱
D.砹的气态氢化物(HAt)比溴化氢的稳定性弱
3、实验题 (11分)X、Y、Z、W和N均是由短周期元素组成的五种化合物。已知五种化合物水溶液的焰色反应均呈黄色,Y、Z和N均由三种元素组成。请根据题目要求回答下列问题。
(1)固体化合物X为浅黄色粉末,该化合物中含有的化学键有________(填序号)。
A.离子键
B.极性共价键
C.非极性共价键
D.氢键
(2)写出X与二氧化碳反应的化学方程式
________________________________________________________________________。
(3)下表为Y与Z实验的部分内容:
序号
| 主要实验步骤及实验现象
|
①
| 在含Y的溶液中,加入稀硫酸放置,产生浅黄色沉淀和无色有刺激性气味的气体,该气体可使品红溶液褪色
|
②
| 在含Z的溶液中,滴加盐酸,开始有白色沉淀,继续滴加盐酸,白色沉淀先增加后消失,然后加入过量的氨水又出现白色沉淀
|
③
| 将实验②最终得到的混合物加热蒸发、灼烧,最终得到白色固体
写出Y与稀硫酸反应的离子方程式
________________________________________________________________________。
(4)写出含0.1 mol Z的溶液与20 mL 5 mol・L-1的盐酸反应的离子反应式
__________________________。实验③加热蒸发、灼烧得到的最终产物主要是________。
(5)化合物W和N可以相互转化:W△CO2+H2ON。若有W和N・xH2O的混合物6.52 g,加热到完全反应后,气体产物通过浓硫酸增重1.71 g,剩余气体通过碱石灰增重1.10 g,则混合物中W的质量为________,N・xH2O的化学式为__________。
4、填空题 (7分)氮元素可以形成多种化合物。
(1)基态氮原子的价电子轨道表示式是 。
(2)已知尿素的结构式为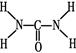 ,则尿素分子中C和N原子的杂化方式分别是、。 ,则尿素分子中C和N原子的杂化方式分别是、。
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被―NH2(氨基)取代形成的另一种氮化物。
①NH3分子的空间构型是;
②肼可用作火箭燃料,燃烧时发生的反应是:
N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g)△H=-1038.7kJ・mol-1
当肼燃烧放出519.35kJ热量时,形成的π键有mol。
5、选择题 已知1~18号元素的离子aW3+、bX+、cY2―、dZ―都具有相同的电子层结构,下列关系正确的是(???)
A.质子数:c>d
B.离子的还原性:Y2―>Z ―
C.氢化物的稳定性:H2Y>HZ
D.原子半径:X<W
|