��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ˮ�ĵ���ƽ�ⲻ����Ӱ���������[???? ]
A.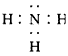
B.13X3+
C.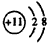
D.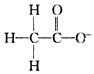
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2��ѡ���� �����£�ijˮ��Һ����ˮ�����c��H+��=1.8��10-12mol/L������Һһ���������ǣ�������
A���ռ���Һ
B��̼��������Һ
C��������Һ
D������������Һ
�ο��𰸣������£���ˮ�����c��H+��=c��OH-���T1��10-7mo
���������
�����Ѷȣ���
3��ѡ���� ���е��뷽��ʽ�У���ȷ���ǣ�������
A��HClO4�TH++ClO4-
B��H2CO3?2H++CO32-
C��H2PO4-+H2O�THPO42-+H3O+
D��NH3?H2O�TNH4++OH-
�ο��𰸣�A
���������
�����Ѷȣ���
4��ѡ���� ������Һһ���ʼ��Ե���
A c(OH��)��c(H��) B c(OH-)��1��10��6mol��L
C ʹ���ȱ�� D pH=8����Һ
�ο��𰸣�A
�����������Һ���������Ҫ�ǿ���Һ�������ӵ�OH��Ũ�ȵ���Դ�С�����c(OH��)��c(H��)�����Լ��ԣ�c(OH��)��c(H��)�������ԣ�c(OH��)��c(H��)�����ԡ�ѡ��BCD����һ���Լ��ԣ����Դ�ѡA��
�����Ѷȣ�һ��
5��ѡ���� ����ʱ����ˮ����ˮ�����c(OH-)=a��pH=1����������ˮ�����c(OH-)=b��0.2 mol��L-1�Ĵ�����0.2 mol��L-1������������Һ�������Ϻ����Һ�У���ˮ�����c(OH-)=c����a��b��c�Ĺ�ϵ��ȷ���� �� ��
A��a>b=c
B��c > a >b
C��c>b>a
D��b>c>a
�ο��𰸣�B
���������ˮ����������ʣ�����ˮ�ĵ��뷽��ʽH2O H����OH����֪����ˮ�м����������������ˮ�ĵ��롣�����ӻ�OH����Ũ��Խ��ˮ�����Ƴ̶�Խ���ε�ˮ��ٽ�ˮ�ĵ��룬����ѡ��B����ȷ�ģ���ѡB��
H����OH����֪����ˮ�м����������������ˮ�ĵ��롣�����ӻ�OH����Ũ��Խ��ˮ�����Ƴ̶�Խ���ε�ˮ��ٽ�ˮ�ĵ��룬����ѡ��B����ȷ�ģ���ѡB��
�����Ѷȣ�һ��