微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 某种牙膏中的摩擦剂是碳酸钙,可以用石灰石(含杂质SiO2)来制备.某同学甲设计了一种制备碳酸钙的方案,其流程图为:
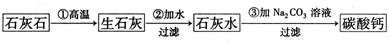
请回答下列问题:
(1)假设第①步反应完全进行,则第②步反应过滤后得到的滤渣的成分为______.
(2)第③步反应不使用CO2,其主要原因是(用离子方程式表示)______
______.
(3)第③步反应使用Na2CO3而不使用NaHCO3,从提高企业经济效益的角度考虑,其原因是______.
(4)某同学乙用石灰石为原料(其他试剂自选),设计了另一种制备碳酸钙的实验方案,请你完成他的实验方案.

乙同学所设计的方案的优点是______.
参考答案:(1)石灰石(含杂质SiO2),依据流程图分析可知,石灰石高
本题解析:
本题难度:一般
2、实验题 工业上制硫酸的设备分为三大部分,一是沸腾炉、二是接触室、三是吸收塔。在沸腾炉内煅烧黄铁矿生成二氧化硫;在接触室内有催化剂存在下二氧化硫进一步与氧气结合,生成三氧化硫;三氧化硫流经吸收塔时,采用98.3% 的浓硫酸吸收,使三氧化硫最终与水化合形成硫酸。下面的装置是仿照工业上制备硫酸的工艺流程设计出来的,用于探究工业上为何采用98.3%的浓硫酸吸收三氧化硫。
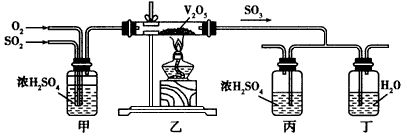
请回答下列问题:
(1)写出沸腾炉内煅烧黄铁矿的反应方程式______________________。
(2)上图中的乙、丙分别相当于工业上制取硫酸装置中的________________、_______________。
(3)丙中的现象为____________,丁中的现象为____________。
(4)下图是压强对SO2平衡转化率的影响
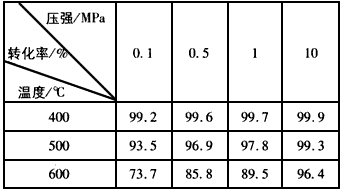
对SO2转化为SO3的反应,增大压强可使转化率____________,之所以通常采用常压操作是因为____________________________。
参考答案:(1)4FeS2+11O2![]() 本题解析:
本题解析:
本题难度:一般
3、选择题 下列实验操作不合理的是
①用NaSCN溶液检验FeCl2溶液是否被氧化
②用溴水检验汽油中是否含有不饱和脂肪烃
③用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸
④仅用蒸馏水鉴别蔗糖、硫酸铜粉末、碳酸钙粉末
⑤配制一定物质的量浓度的溶液,需要的玻璃仪器只有容量瓶和烧杯
⑥测溶液大致的pH:用干燥玻璃棒蘸取溶液滴在pH试纸上,与标准比色卡对照
⑦在250 mL烧杯中,加入216 mL水和24 g NaOH固体,配制10%NaOH溶液
A.①④⑥
B.③⑤⑦
C.②④⑤
D.②⑥⑦
参考答案:B
本题解析:酯化反应是可逆反应,用乙醇和浓硫酸不但不能除去乙酸乙酯中的少量乙酸,还引入了新的杂质,③不合理;配制一定物质的量浓度的溶液,需要的玻璃仪器有容量瓶、烧杯、玻璃棒、胶头滴管,⑤错;烧杯中所盛液体不宜超过其体积的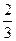 ,在250 mL烧杯中加入216 mL水,已经超过了规定的容量,⑦不合理。
,在250 mL烧杯中加入216 mL水,已经超过了规定的容量,⑦不合理。
本题难度:简单
4、实验题 黄铁矿(主要成分为FeS2)是我国大多数硫酸厂制取硫酸的主要原料。某化学学习小组对某黄铁矿石进行如下实验探究。
[实验一]测定硫元素的含量。
Ⅰ、将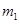 g该黄铁矿样品放入如图1所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为:4FeS2+11O2
g该黄铁矿样品放入如图1所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为:4FeS2+11O2 2Fe2O3+8SO2?
2Fe2O3+8SO2?
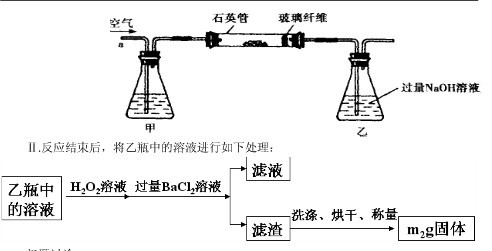
Ⅱ、反应结束后,将乙瓶中的溶液进行如图2所示处理。
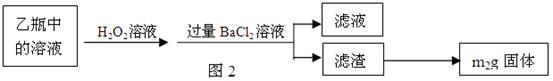
[实验二]测定铁元素的含量。
Ⅲ、测定铁元素含量的实验步骤如图3所示:
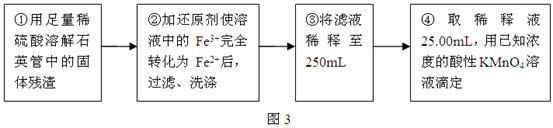
问题讨论:
 ??
??
(1)Ⅰ中,甲瓶内所盛试剂是???????溶液。乙瓶内发生反应的离子方程式有:
????????????????????????????、????????????????????????????。
(2)Ⅱ中的滤渣在称量前还应进行的操作是???????????????????????????????????。
(3)Ⅱ中,所加H2O2溶液(氧化剂)需足量的理由是?????????????????????????。
(4)Ⅲ的步骤③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有????????。
写出④中反应的离子方程式??????????????????????????????????。
(5)该黄铁矿中硫元素的质量分数为?????????????????。
参考答案:(1)NaOH (2分)  本题解析:(1)由于空气中含有CO2和水蒸气,所以必须除去,以防止干扰后面的SO2的吸收,因此盛放的是氢氧化钠溶液。SO2是酸性氧化物,能被氢氧化钠溶液吸收,反应的方程式是SO2+2OH-=SO32-+H2O。又因为亚硫酸钠极易被氧气氧化,所以还可能发生反应2SO32-+O2=2SO42-。
本题解析:(1)由于空气中含有CO2和水蒸气,所以必须除去,以防止干扰后面的SO2的吸收,因此盛放的是氢氧化钠溶液。SO2是酸性氧化物,能被氢氧化钠溶液吸收,反应的方程式是SO2+2OH-=SO32-+H2O。又因为亚硫酸钠极易被氧气氧化,所以还可能发生反应2SO32-+O2=2SO42-。
(2)沉淀在称量之前还需要洗涤和干燥。
(3)为了使溶液中的SO32-完全被氧化生成SO42-,加入的过氧化钠应该是过量的。
(4)由于要稀释至250ml,所以还需要250ml容量瓶。酸性高锰酸钾溶液具有氧化性,能氧化亚铁离子,反应的方程式是5Fe2+ + 2MnO4-+16H+==5Fe3++2Mn2++8H2O。
(5)硫酸钡的质量是m2g,物质的量是m2/233mol,则SO2的物质的量是m2/233mol,所以硫元素的质量分数是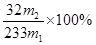 。
。
本题难度:一般
5、实验题 某班同学用如图所示的装置测定空气里氧气的含量。药匙上放少量钠,烧杯中装满水,先用弹簧夹夹住橡胶管。点燃钠,伸入瓶中并塞上瓶塞。待钠熄灭并冷却后,打开弹簧夹,观察广口瓶内水面变化情况。
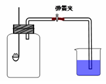
(1)写出燃烧匙中发生反应的化学方程式:???????????????????????????????,将该生成物伸入瓶底的水中,生成的氧化产物与还原产物物质的量之比为:?????。
(2)实验完毕,广口瓶内水面上升明显小于空气体积的1/5,对这一现象解释正确的是:?????
a.该同学可能未塞紧瓶塞,导致钠熄灭时外界空气进入瓶内
b.该同学可能使用钠的量不足
c.该同学可能没夹紧弹簧夹,钠燃烧时部分空气受热从导管逸出
d.该同学可能插入燃烧匙太慢,塞紧瓶塞前瓶内部分空气受热逸出
参考答案:(1)2Na+O2 本题解析:
本题解析:
试题分析:该实验利用金属钠燃烧消耗集气瓶集气瓶内氧气,压强减小,回复室温后,打开弹簧夹,烧杯内的水进入集气瓶,水的体积就是消耗掉氧气的体积。金属钠燃烧反应生成Na2O2,2Na2O2+2H2O=4NaOH+O2,Na2O2既是氧化剂又是还原剂,氧化产物是氧气,NaOH有一半是还原产物,氧化产物与还原产物物质的量之比为1:2,最后水的体积小,说明所测结果体积偏小,a导致外界空气进入装置,倒流回去的水偏少,正确;b、钠不足,没有把氧气消耗完,所测体积少,正确;c、空气溢出,水倒流的应该更多,错误;d、空气溢出,水倒流的应该更多,错误。
本题难度:一般