��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1�������� ��Fe2O3����150mLϡH2SO4�У���Fe2O3��ȫ�ܽ�������ۣ���������3.36L����״��������Һ�в�����Fe��Fe3+����֪��������ۺ���������19.2g�����㣺
��1��Fe2O3������Ϊ??????????????g ��
��2��ϡH2SO4���ʵ���Ũ��Ϊ??????????????��
�ο��𰸣�Fe2O3��8g��2�֣��� c(H2SO4) ��2mol/L
��������������ۡ�Fe2O3�����ʵ����ֱ�Ϊx��y
�����ʵ���������56x+160y=19.2
�ڷ�Ӧ�����У����������ҺΪFeSO4��Һ���ɵ��ӵĵ�ʧ�غ�ɵã�2x=2y+
���x=0.2mol?? y=0.05mol
��Fe2O3������Ϊ0.05��160=8g
����Ԫ�ص��غ��֪��������
�����Ѷȣ���
2������� ��1.000gFeC2O4��2H20������Ʒ�������ط������н������ط������y�������ط������ߣ���Ʒ�������¶ȱ仯�����ߣ�����ͼ��ʾ��
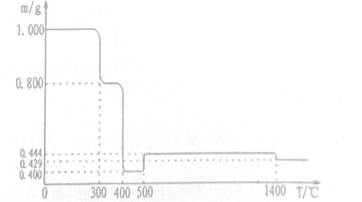
��֪���ٲ��������ȷֽ��ų�̼���������5000C֮ǰ�������ط����ǵ���Ʒ�ش���Ar�������У�5000Cʱ����Ʒ���������ͨ�����������գ�
(1)3000Cʱ����Ʒ��ˮ�Ĺ��̣���ȷ��3500Cʱ��Ʒ�Ƿ���ˮ��ȫ_____ (���"������жϵ�������____(Ҫ��д��������̣���
(2 ) 4000Cʱ�����仯�Ļ�ѧ����ʽ��_______��
(3) ��6000Cʱ��Ʒ���в����Ĺ������������ȴ�����£�����ù����м���һ������ϡ����պ���ȫ�ܽ⣬��pH��ֽ���������Һ��PH��3����ԭ����____(�����ӷ���ʽ�ش𣩣������Һ�еμ�����NaOH��Һ���ɺ��ɫ�������y�ô�ʱ��Һ����Ԫ��������Ũ��Ϊ4.0x10-11mol/L�����ʱ��Һ��pH��_______(��֪��Ksp[Fe(OH)2]��8.0��10��16��Ksp[Fe(OH)3]��4.0��10��38)
(4) ��15000Cʱ��Ʒ���в����Ĺ������������ȴ����ϡ�����ܽ��һ�ػ�ɫ��Һ��ȡ��������Һ�μ�KSCN,��Һ�Ժ�ɫ����ȡ��������Һ�μ�K3[Fe(CN)6)(���軯�أ���Һ������������ɫ��������д��ͼ��14000Cʱ������Ӧ�Ļ�ѧ����ʽ_________ ,����������ɫ���������ӷ�Ӧ����ʽ______��
�ο��𰸣���1���ǣ�2�֣���2��FeC2O4 ���������
���������
�����������1����Ʒ�ֽ�ķ���ʽ��
FeC2O4��2H2O FeC2O4��(2��n)H2O��nH2O
FeC2O4��(2��n)H2O��nH2O
180g????????????????????????????18n
1.000g???????????????????????��1.000g��0.800g��
���n��2��������
�����Ѷȣ�һ��
3��ѡ���� Ϊ�˳�ȥFeCl2��Һ�л��е�����FeCl3����õķ����������Һ��? (???? )
A��ͨ������
B������Zn
C������Fe
D������Cu
�ο��𰸣�C
������������ӵĻ���ԭ���Dz���������������ԭ������ü���Fe����Ӧ����ˣ��õ�ֻ��Fe2+��
�����Ѷȣ�һ��
4��ʵ���� ��6�֣�ijѧ��������������ȼ�յ�ʵ��ʱ��ʹ����ո�µ�ͭ��ȼ�ճף�����ȼ��ʱ�����˹۲쵽�а����⣬����������ɫ���̣���˵���������Ļ�ѧ����ʽΪ
__________________��___________________________����������Ӧ�õ��Ĺ�������ˮ���ټ���NaOH��Һ������������ɫ�������÷�Ӧ�����ӷ���ʽΪ��
__________________________��
�ο��𰸣�Cu+Cl2 ����������ƺ�ͭ������������Ӧ��ǰ�������Ȼ��ƣ����������Ȼ�ͭ�����ֹ��嶼��������ˮ������Һ���������ƻ�ϣ��Ȼ��Ʋ���Ӧ���Ȼ�ͭ�������������ɫ������
����������ƺ�ͭ������������Ӧ��ǰ�������Ȼ��ƣ����������Ȼ�ͭ�����ֹ��嶼��������ˮ������Һ���������ƻ�ϣ��Ȼ��Ʋ���Ӧ���Ȼ�ͭ�������������ɫ������
�����Ѷȣ���
5��ѡ���� ����Fe��FeO��Fe2O3��ɵĻ�����м���100 mL 2 mol��L-1�����ᣬǡ��ʹ�������ȫ�ܽ⣬���ų�448 mL���壨��״��������ʱ��Һ����Fe3+���ڡ��������ж���ȷ����
��???��
A����������������ʷ�Ӧ�����ĵ���������ʵ���֮��Ϊ1��1��3
B��������Fe2O3�����ʵ�����ȷ������Fe��FeO�����ʵ�����
C��������FeO�����ʵ�����ȷ������Fe��Fe2O3�����ʵ�����
D����Ӧ��������Һ�е�Fe2+��Cl-�����ʵ���֮��Ϊ1��3
�ο��𰸣�C
��������������⣬���ڷ�Ӧ��������ų�����Һ�в�����Fe3+����n(Fe)��n(Fe2O3)����FeO�����ʵ����ء����ղ���ΪFeCl2����n(Fe2+)=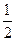 n(Cl-)��
n(Cl-)��
�����Ѷȣ���