微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某研究小组用NaOH溶液吸收二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法.其中阴阳膜组合循环再生机理如图,则下列有关说法错误的是( )
A.阳极区酸性增强
B.阴极区电极反应式为:2H++2e-=H2↑
C.diluent和concentrated的中文含义为浓缩的、稀释的
D.该过程中的副产品主要为H2SO4
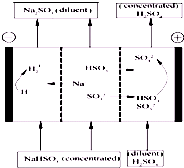
参考答案:A、电解池中,阳极不是活泼电极时,放电的是氢氧根,浓度减小,
本题解析:
本题难度:简单
2、选择题 研读下图,下列判断不正确的是:(????? )

A.K 闭合时,d电极反应式:
B.当电路中转移0.2mol电子时,I中消耗的H2SO4为0.2 mol
C.K闭合时,II中SO42-向c电极迁移
D.K闭合一段时间后,II可单独作为原电池,d电极为正极
参考答案:C
本题解析:
答案:C
A、正确,K 闭合时,d电极为电解池的阳极
B、正确,由方程式可知:PbO2+2H2SO4+Pb=2PbSO4+2H2O,每转移1mol电子,消耗1molH2SO4
C、不正确,K闭合时,II中SO42-向d电极迁移;
D.正确,K闭合一段时间后,II被充电。
本题难度:简单
3、选择题 下列有关工业生产的叙述正确的是
A.合成氨生产过程中将NH3液化分离,会降低反应速率,可提高N2、H2的转化率
B.从海水中提镁过程中,电解熔融MgO可制备Mg
C.电解精炼铜时,同一时间内阳极溶解固体的质量比阴极析出固体的质量小
D.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室
参考答案:C
本题解析:
试题分析:A、合成氨生产过程中将NH3液化分离,会降低逆反应速率,但不会降低正反应速率,A错误;B、制备Mg应电解熔融MgCl2,B错误;C、电解精炼铜,阳极除了Cu失电子,还有比铜活泼的锌、镍、铁失电子,C正确;D、电解饱和食盐水时用离子交换膜法,防止阳极室产生的Cl2进入阴极室,D错误;答案选C。
考点:考查化学与化工生产。
本题难度:一般
4、填空题 Ⅰ.通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。下表为一些化学键的键能数据
化学键
| Si-Si
| O=O
| Si-O
|
键能/kJ・mol-1
| a
| b
| c
写出硅高温燃烧的热化学方程式 。
Ⅱ.利用太阳光分解水制氢是未来解决能源危机的理想方法之一。某研究小组设计了如右图所示的循环系统实现光分解水制氢。反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe3+等可循环使用。写出下列电解池中总反应的离子方程式:

电解池A 。
电解池B 。
(2)若电解池A中生成3.36 L H2(标准状况),计算电解池B中生成Fe2+的物质的量为 mol。
Ⅲ.在一定的温度下,把2体积N2和6体积H2分别通入一个带活塞的体积可变的容器中,活塞的一端与大气相通容器中发生如下反应:N2(g)+3H2(g) 2NH3(g);△H<0,反应达到平衡后,测得混合气体为7体积。 2NH3(g);△H<0,反应达到平衡后,测得混合气体为7体积。

请据此回答下列问题:
(1)保持上述反应温度不变,设a、b、c分别表示加入的N2、H2 和NH3的体积,如果反应达到平衡后混合气体中各物质的量仍与上述平衡时完全相同。
①a=1,c=2,则b= 。在此情况下,反应起始时将向 反应方向(填“正”或“逆”)进行。
②若需规定起始时反应向逆方向进行,则c的取值范围是 。
(2)在上述恒压装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是 ,原因是 。
参考答案:Ⅰ.Si(s)+O2(g) 本题解析: 本题解析:
试题分析:Ⅰ.硅是原子晶体,平均1个硅原子形成2个Si-Si键。二氧化硅是原子晶体,平均1个硅原子形成4个Si-O键。又因为反应热等于断键吸收的能量与形成化学键所放出的能量的差值,因此硅高温燃烧的热化学方程式为Si(s)+O2(g) SiO2(s) △H=(2a+ b - 4c)kJ/mol。 SiO2(s) △H=(2a+ b - 4c)kJ/mol。
Ⅱ.(1)电解池左边放出氢气,氢离子在此得到电子,发生还原反应,则碘离子失去电子发生氧化反应,故A池中总反应式为2H+ +2I-=H2↑ + I2;电池右侧放出氧气,说明溶液中的氢氧根失去电子发生氧化反应,则溶液中的铁离子得到电子发生还原反应,因此B池总反应式为4Fe3+ + 2H2O=4Fe2+ + O2↑+ 4H+。(2)若电解池A中生成3.36 L H2(标准状况),其中氢气的物质的量是3.36L÷22.4L/mol=0.15mol,转移电子0.3mol,所以根据得失电子守恒可知B池中生成亚铁离子的物质的量是0.3mol。
Ⅲ.(1)①反应达到平衡后混合气体中各物质的量仍与上述平衡时完全相同,恒温恒压条件下,采用极限分析法,c体积的氨气完全转化为氮气和氧气之比是1:3,所以只要a:b=2:6,则b=3a=3,因反应前混合气体为8体积,反应后混合气体为7体积,体积差为1体积,由差量法可解出平衡时氨气为1体积;而在起始时,氨气的体积为c=2体积,比平衡状态时大,为达到同一平衡状态,氨的体积必须减小,所以平衡逆向移动;
②若需让反应逆向进行,由上述①所求出的平衡时氨气的体积为1可知,氨气的体积必须大于1,最大值则为2体积氮气和6体积氢气完全反应时产生的氨气的体积,即为4体积,则1<c≤4;
(2)根据6.5<7可知,上述平衡应向体积缩小的方向移动,即向放热方向移动,所以采取降温措施,这是由于降低温度平衡向正反应方向移动,气体总分子数减少。
考点:考查热化学方程式的书写、电化学原理的应用、以及可逆反应的有关计算与判断
本题难度:困难
5、选择题 下列叙述正确的是
A.氢氧燃料电池中O2通入负极
B.铅蓄电池在放电时,其负极的电极反应为:Pb-2e=Pb2+
C.碱性锌锰电池在工作时,电解质中的OH-移向正极
D.在海轮外壳镶嵌锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
参考答案:D
本题解析:
试题分析:A.氢氧燃料电池中O2通入正极,错误;B.铅蓄电池在放电时,其负极的电极反应为:Pb-2e+SO42-=PbSO4↓,错误;C碱性锌锰电池在工作时,电解质中的OH-移向正电荷较多的负极,错误;D.在海轮外壳镶嵌锌块,由于金属活动性Zn>Fe,所以首先被腐蚀的是Zn,因此轮船就得到你了保护,保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法,正确。
考点:考查原电池、电解池的反应原理及应用的知识。
本题难度:一般
|