��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �ڼ�������������У�����֤������������ʵ���
A��1mol/L�ļ�����Һ��c��H+��ԼΪ1��10��2 mol/L
B����������ˮ�������������
C��1mol/L�ļ�����Һ10mLǡ����10mL1mol/L��NaOH��Һ��ȫ��Ӧ
D��������Һ�ĵ����Ա�������
�ο��𰸣�A
���������
���������
A��������һԪ�ᣬ������Ũ��С�����Ũ�ȣ�˵���������ȫ���룬�϶���������ʣ���A�������⣻
B���ܽ���������ǿ���أ���B�������⣻
C������Ƿ�ǡ����ȫ��Ӧ��ǿ���أ���C�������⣻
D��δָ���Ƿ�����ͬŨ�ȵ������ᣬ���ӵ������ϲ���֤���������ǿ������D�������⡣
���㣺������ʵ��ж�����
���������⿼����������ʵ��ж����ݣ��ѶȲ�����ʱץסһ���ؼ���Ҫ֤��һ���������ᣬ��Ҫ֤��������ȫ���롣Ҫ����ע����ǣ�����ʵ�ǿ�����ܽ��ԡ�������û�б�Ȼ����ϵ��
�����Ѷȣ�һ��
2��ѡ���� ��ˮϡ��0.5mol?L-1�Ĵ��ᣨCH3COOH����Һ��������ˮ�������Ӷ�������ǣ�������
��H+�����ʵ���
��C��H+��
��C��H+��/C��CH3COO-��
��C��CH3COOH��/C��CH3COO-��
��C��OH-��
A���٢ۢ�
B���٢ܢ�
C���ڢ�
D���ۢ�
�ο��𰸣����ᣨCH3COOH����Һ�д�����������ʴ��ڵ���ƽ�⣬CH
���������
�����Ѷȣ���
3��ѡ���� ����������ȷ����[???? ]
A����ϡ��ˮ��μ���ϡ�����У�����ҺpH=7ʱ��c(SO42-)��c(NH4+)
B�����ִ�����Һ�����ʵ���Ũ�ȷֱ�Ϊc1��c2��pH�ֱ�Ϊa��a+1����c1=10c2
C��pH=11��NaOH��Һ��pH=3�Ĵ�����Һ�������ϣ�����ʯ����Һ�ʺ�ɫ
D����0��1 mol/L�İ�ˮ�м�����������粒��壬����Һ��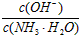 ����
����
�ο��𰸣�C
���������
�����Ѷȣ�һ��
4��ѡ���� ��NaOH��Һ�백ˮ��pH���������ͬʱ������������ȷ����[???? ]
A������Һ�����ʵ���Ũ����ͬ
B������Һ��c(H��)��ͬ
C����ͬŨ�������к�ʱ��������������ͬ
D�������¶�10�棬����pH�����
�ο��𰸣�B
���������
�����Ѷȣ�һ��
5������� �����Ź㷺����;��������ڻ��ʡ����ᡢ�ϳ���ά�ȹ�ҵ����������ˮ��Һ�д��ڵ���ƽ�⣬���õ��볣��Kb�͵���Ȧ���������ʾ�����̶ȣ�Kb�ͦ����õIJⶨ��������һ���¶�ʱ����ȼƲⶨһϵ����֪Ũ�Ȱ�ˮ��pH���ɵø�Ũ�Ȱ�ˮ��Ӧ��c��OH-����Ȼ��ͨ��������ø���Ӧ�Ħ�ֵ��Kbֵ��
������ij��ѧ��ѧ��ȤС����25��ʱ�ⶨһϵ��Ũ�Ȱ�ˮ��pH����Ӧ��c��OH-����
[�������Լ�]��ȼơ�50mL��ʽ�ζ��ܡ�100mL�ձ���0.10mol?L-1?��ˮ
[ʵ������]�����������
| �ձ��� | V��ˮ?��mL�� | Vˮ��mL�� | c?��NH3?H2O��?��mol?L-1�� | c��OH-�� | Kb | ��
1
50.00
0.00
1.34��10-3
2
25.00
25.00
9.48��10-4
3
5.00
45.00
4.24��10-4
�����������Ϣ�ش��������⣺
��1��25��ʱ����ˮ�ĵ��볣����Kb��______��ͨ���������õ����ݺͼ�������˵�����볣�����������������ʵij�ʼŨ�ȵĹ�ϵ______
��2����0.10mol?L-1����ֱ�ζ�20.00mL0.10mol?L-1��NaOH��Һ��20.00mL0.10mol?L-1��ˮ���õĵζ��������£�
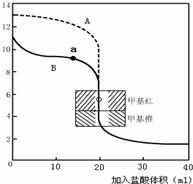
��ָ������ζ���ˮ������Ϊ______����A��B������д������a������Ӧ����Һ�и�����Ũ���ɴ�С������˳��______��
��3��Һ����Ϊһ��DZ�ڵ��������ȼ����Խ��Խ���о���Ա���ӣ����ڰ�ȫ�ԡ��۸�ȷ���ϻ�ʯȼ�Ϻ���ȼ�����Žϴ�����ƣ�����ȼ�����������صķ�Ӧ�У�
4NH3��g��+3O2��g��=2N2��g��+6H2O��l����H1��
4NH3��g��+5O2��g��=4NO��g��+6H2O��l����H2��
4NH3��g��+6NO��g��=5N2��g��+6H2O��l����H3��
��д������������Ӧ�С�H1����H2����H3����֮���ϵ�ı���ʽ����H1=______��
��4��Allis-Chalmers���칫˾���ֿ����ð���Ϊȼ�ϵ�ص�ȼ�ϣ����ܷ�ӦʽΪ4NH3+3O2=2N2+6H2O�������ϵĵ缫��ӦʽΪO2+
2H2O+4e-=4OH-�����ϵĵ缫��ӦʽΪ______��
�ο��𰸣���1����NH3?H2O�TNH4++OH-����һ��ʵ���е�Kb
���������
�����Ѷȣ�һ��
|