��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��10�֣��о�NO2��SO2 ��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
��1�����÷�Ӧ6NO2�� 8NH3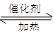 7N2��12 H2O�ɴ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״������ L��
7N2��12 H2O�ɴ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״������ L��
��2����֪��2SO2��g��+O2��g��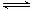 2SO3��g�� ��H=��196.6 kJ��mol-1
2SO3��g�� ��H=��196.6 kJ��mol-1
2NO��g��+O2��g��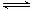 2NO2��g�� ��H=��113.0 kJ��mol-1
2NO2��g�� ��H=��113.0 kJ��mol-1
��ӦNO2��g��+SO2��g��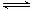 SO3��g��+NO��g���Ħ�H= kJ��mol-1��
SO3��g��+NO��g���Ħ�H= kJ��mol-1��
��3�����������ֳư�������أ��ŵ�ʱ���ܷ�ӦΪ��Fe+Ni2O3+3H2O= Fe(OH)2+2Ni(OH)2
����طŵ�ʱ�������缫��ӦʽΪ ��
�ο��𰸣�����10�֣�
��1��6.72��3�֣�
��2��-
���������
��NO2�ڱ�״����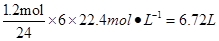
�Ƣ�2SO2��g��+O2��g��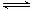 2SO3��g�� ��H=��196.6 kJ��mol-1
2SO3��g�� ��H=��196.6 kJ��mol-1
��2NO��g��+O2��g��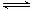 2NO2��g�� ��H=��113.0 kJ��mol-1
2NO2��g�� ��H=��113.0 kJ��mol-1
����
�����Ѷȣ�����
2��ѡ���� ȼ�յ����ȼ��(��CO��H2��CH4��)������(�����)��Ӧ����ѧ��ת��Ϊ���ܵ�װ�ã��������Һ��ǿ��(��KOH)��Һ��������ڼ���ȼ�յ�ص�˵������ȷ����
A��������ӦʽΪO2+2H2O+4e��=4OH��
B��������ӦʽΪCH4+10OH����8e��=CO32��+7H2O
C�����ŷŵ�Ľ��У���Һ��pHֵ����
D������ȼ�յ�ص����������ʱȼ���ȼ�յĴ�
�ο��𰸣�C
���������ԭ����и���ʧȥ���ӣ������õ����ӣ�����ѡ��AB��ȷ�����������缫��Ӧʽ���Ӽ��õ��ܷ�ӦʽΪCH4��2O2=CO32����3H2O�������Һ�ļ����ǽ��͵ģ�C����ȷ��D����ȷ�ģ����Դ���C��
�����Ѷȣ���
3��ѡ���� ��ͼ��һ�ֺ�������������ϵͳԭ��ʾ��ͼ������˵����ȷ����
 [???? ]
[???? ]
A����ϵͳ��ֻ����3����ʽ������ת��
B��װ��Y�и����ĵ缫��ӦʽΪ��O2+2H2O+4e-=4OH-
C��װ��X��ʵ��ȼ�ϵ�ص�ȼ�Ϻ�����������
D��װ��X��Y�γɵ���ϵͳ��ʵ�����ʵ����ŷţ�����ʵ�ֻ�ѧ������ܼ����ȫת��
�ο��𰸣�C
���������
�����Ѷȣ�һ��
4������� ������(CH3OCH3)����Ϊ21���͵�����ȼ�ϣ���δ�������������ȼ�͡�ʯ��Һ�������� ��ú���ȣ��г�ǰ����Ϊ����������࣬��Ч�����������Ļ������ܡ� ��ҵ���ƶ���������һ���¶�(230~ 280��)��ѹǿ(2.0~10.0 MPa)�ʹ��������½��еģ���Ӧ���з��������з�Ӧ��
CO(g)+2H2(g)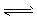 CH3OH(g) ��H1=-90.7 kJ . mol-1��
CH3OH(g) ��H1=-90.7 kJ . mol-1��
2CH3OH(g)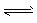 CH3OCH3(g)+H2O(g) ��H2 =-23.5 kJ . mol-1 ��
CH3OCH3(g)+H2O(g) ��H2 =-23.5 kJ . mol-1 ��
CO(g)+H2O(g)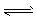 CO2(g)+H2(g) ��H3=-41.2 kJ . mol-1 ��
CO2(g)+H2(g) ��H3=-41.2 kJ . mol-1 ��
(1)��Ӧ���е��ܷ�Ӧ�ɱ�ʾΪ3CO(g)+3H2(g)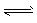 CH3OCH3(g)+CO2(g)����÷�Ӧ�ġ�H ___��ƽ�ⳣ������ʽΪ___���ں��¡��ɱ��ݻ����ܱ������н���������Ӧ������ѹǿ�������ѵIJ��ʻ�____�������ߡ����ͻ䣩��
CH3OCH3(g)+CO2(g)����÷�Ӧ�ġ�H ___��ƽ�ⳣ������ʽΪ___���ں��¡��ɱ��ݻ����ܱ������н���������Ӧ������ѹǿ�������ѵIJ��ʻ�____�������ߡ����ͻ䣩��
(2)������̼��һ����Ҫ���������壬���ٶ�����̼���ŷ��ǽ������ЧӦ����Ч;����Ŀǰ���ɶ�����̼�ϳɶ����ѵ��о�������ȡ�����ش��չ���仯ѧ��Ӧ����ʽΪ2CO2(g)+6H2(g) 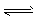 CH3OCH3(g)+3H2O(g) ��H>0�� �÷�Ӧ�ں��¡�����㶨���ܱ������н��У����в�����Ϊ�÷�Ӧ�Ѵﵽ��ѧƽ��״̬���ж����ݵ���____��
CH3OCH3(g)+3H2O(g) ��H>0�� �÷�Ӧ�ں��¡�����㶨���ܱ������н��У����в�����Ϊ�÷�Ӧ�Ѵﵽ��ѧƽ��״̬���ж����ݵ���____��
A�������ڻ��������ܶȲ���
B�������ڻ�������ѹǿ���ֲ���
C�������ڻ�������ƽ��Ħ���������ֲ���
D����λʱ��������2 mol CO2��ͬʱ����1 mol������
(3)�����������ȼ����Ϊ1 455 kJ��mol-1����ҵ���úϳ���(CO��H2)ֱ�ӻ��Ӻϳɶ����ѡ� �����й�������ȷ����____��
A�������ѷ����к����ۼ�
B����������Ϊ����ȼ�ϲ��������Ⱦ��
C�����������Ҵ���Ϊͬϵ��
D����ʾ������ȼ���ȵ��Ȼ�ѧ����ʽΪCH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(g) ��H=-1 455 kJ��mol-1
(4)��ɫ��Դ��ֱ�Ӷ�����ȼ�ϵ�ء��Ĺ���ԭ��ʾ��ͼ��ͼ��ʾ������Ϊ___����A�缫��B�缫����д��A�缫�ĵ缫��Ӧʽ��___ ��
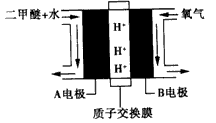
�ο��𰸣�(1) -246.1 kJ . mol-1? ��![]()
���������
�����Ѷȣ�һ��
5��ѡ���� ij���Ϳɳ���أ��ܳ�ʱ�䱣���ȶ��ķŵ��ѹ,�õ�ص��ܷ�ӦΪ��
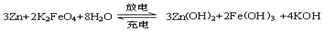
������˵������ȷ���ǣ�



A���ŵ�ʱ������ӦΪ��Zn-2e�C+2OH�C=Zn(OH)2
B���ŵ�ʱ������ӦΪ��FeO42�C+4H2O+3e�C=Fe(OH)3+5OH�C
C�����ʱ����������Һ�ļ��Լ���
D���ŵ�ʱÿת��3 mol���ӣ�������1 molK2FeO4������
�ο��𰸣�D
����������ŵ�ʱ����������Ӧ��Zn-2e�C+2OH�C=Zn(OH)2 ���ŵ�ʱ������ԭ��ӦΪ��FeO42�C+4H2O+
3e�C=Fe(OH)3+5OH�C��AB��ȷ��ÿת��3 mol���ӣ�������1 molK2FeO4����ԭ�����ʱ�������������ļ��Լ�����C��ȷ��D����
�����Ѷȣ�һ��