微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法不正确的是(???)
A.一个反应能否自发进行取决于该反应放热还是吸热
B.同一条件下不同物质有不同的熵值,其体系的混乱程度越大,熵值越大
C.焓变是一个与反应能否自发进行有关的因素,多数能自发进行的反应都是放热反应
D.一个反应能否自发进行,与焓变和熵变的共同影响有关
参考答案:A
本题解析:
试题分析:根据△G=△H-T・△S可知,只要△G<0,反应就一定是自发进行的,所以选项B、C、D都是正确的,而选项A是不正确的,答案选A。
点评:熵是与体系混乱度有关系的一种物理量,其体系的混乱程度越大,熵值越大。对于同一种物质,在气态时熵值最大、液态其次、固态是最小。
本题难度:简单
2、选择题 归纳法是
参考答案:
本题解析:
本题难度:困难
3、选择题 自发进行的反应一定是( ? )
A.吸热反应
B.放热反应
C.熵增加反应
D.熵增加或者放热反应
参考答案:D
本题解析:
本题难度:简单
4、选择题 可逆反应2NO2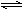 2NO+O2在恒容密闭容器中反应,能说明反应已达到平衡状态的是
2NO+O2在恒容密闭容器中反应,能说明反应已达到平衡状态的是
①单位时间内生成n mo1 O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n molNO
③混合气体的颜色不再改变
④c(NO2)∶c(NO)∶c(O2)=2∶2∶1
⑤混合气体的压强保持不变
⑥各物质的浓度相等
A.①③⑤
B.②④⑤⑥
C.①③④⑤⑥
D.①②③④⑤⑥
参考答案:A
本题解析:单位时间内生成n mo1 O2的同时生成2n mol NO2,和单位时间内生成n mol O2的同时消耗2n molNO已达到平衡状态,混合气体的颜色不再改变代表各组分的浓度保持不变,压强也不变也达到了平衡状态。浓度相等和速率为方程式的比值不是平衡状态。
本题难度:一般
5、选择题 下列叙述正确的是 (???? )
A.反应NH3(g)+HCl(g)=NH4Cl(s)△H<0,在任何条件下均能自发进行
B.铅蓄电池在放电过程中,负极质量减小,正极质量增加
C.温度一定时,水的离子积常数Kw不随外加酸(碱)浓度的改变而改变
D.由于Ksp(BaSO4)小于Ksp(BaCO3),因此不可能使BaSO4沉淀转化为BaCO3沉淀
参考答案:C
本题解析:A中是熵值减小的反应,根据△G=△H-T・△S可知,反应在低温下自发进行,不正确。B不正确,铅蓄电池在放电过程中,负极质量和极质量均是增加的。能否生成BaCO3沉淀,关键是溶液中c(Ba2+)・c(CO32-)>Ksp(BaCO3),所以D是不正确。因此正确的答案是C。
本题难度:一般