微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子方程式与所述事实相符且正确的是( )
A.在强碱性溶液中,次氯酸钠将Mn2+氧化成MnO2:Mn2++ClO-+H2O=MnO2↓+Cl-+2H+
B.用稀硝酸清洗做过银镜反应的试管:Ag+NO +4H+===Ag++NO↑+2H2O
+4H+===Ag++NO↑+2H2O
C.向FeBr2溶液中通入过量的Cl2:2Fe2++2Br-+2Cl2===2Fe3++Br2+4Cl-
D.用铁棒作阴极、炭棒作阳极电解饱和氯化钠溶液: 2Cl-+2H2O H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
参考答案:D
本题解析:
试题分析:A.在强碱性溶液中H+不能大量存在,错误;B.电子部守恒,电荷也不守恒,用稀硝酸清洗做过银镜反应的试管的蜡烛方程式应该是:3Ag+NO +4H+===3Ag++NO↑+2H2O,错误;C.不符合微粒的物质的量的比,应该是: 2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl-,错误;D.反应符合事实,拆写符合离子方程式的书写原则,正确。
+4H+===3Ag++NO↑+2H2O,错误;C.不符合微粒的物质的量的比,应该是: 2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl-,错误;D.反应符合事实,拆写符合离子方程式的书写原则,正确。
考点:考查离子方程式的书写的正误判断的知识。
本题难度:一般
2、选择题 将CO2气体缓缓通入到含有等物质的量的KOH、Ba(OH)2和KAlO2的混合溶液中,直至过量,生成的沉淀的物质的量与所通CO2的体积关系如图所示(假设每步反应均完全)。下列关于整个反应进程中的各种描述不正确的是
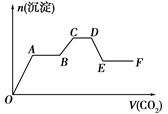
A.A→B段与C→D段所发生的反应相同
B.B→C段反应的离子方程式是:2AlO2
参考答案:
本题解析:
本题难度:一般
3、选择题 下列反应的离子方程式书写不正确的是( )
A.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:
Ba2++2OH-+H++ SO42- + NH4+= BaSO4↓+ NH3?H2O+H2O
B.将少量SO2气体通入NaClO溶液中:SO2+H2O+ ClO-=SO42-+Cl-+2H+
C.硫化钠的水解:S2-+ H2O HS- + OH-
HS- + OH-
D.NaHCO3溶液中滴加少量澄清石灰水:2HCO3-+Ca2++2OH-= CaCO3↓+2H2O+ CO32-
参考答案:B
本题解析:
试题分析:A、硫酸根离子与钡离子刚好完全沉淀时,说明氢氧化钡与NH4HSO4的物质的量之比是1:1,二者反应生成硫酸钡沉淀、水、一水合氨,正确;B、少量的二氧化硫与次氯酸根离子发生氧化还原反应,生成硫酸根离子和氯离子及氢离子,后氢离子与过量的次氯酸根离子结合生成次氯酸,错误;C、S2-发生水解生成HS- 、OH-,正确;D、少量的石灰水与过量的碳酸氢钠溶液反应,氢氧根离子与碳酸氢根离子完全反应生成碳酸根离子和水,生成的碳酸根离子与钙离子结合生成碳酸钙沉淀,所以最终的产物是碳酸钙、碳酸根离子、水,正确,答案选B。
考点:考查离子方程式书写的判断
本题难度:一般
4、选择题 下列离子方程式正确的是
A.硫酸铜溶液与氢氧化钡溶液反应:Ba2+ + SO42- =BaSO4↓
B.用醋酸溶解水垢中的Mg(OH)2:2H+ + Mg(OH)2=Mg2++2H2O
C.工业上用氨水吸收二氧化硫:2OH- + SO2 = SO32- + H2O
D.在NaOH溶液中加入少量Ca(HCO3)2溶液:Ca2++2HCO3 - +2OH - = CaCO3↓+ CO32- + 2H2O
参考答案:D
本题解析:
试题分析:A、硫酸铜与氢氧化钠溶液混合,除生成硫酸钡沉淀外,还有氢氧化铜沉淀生成,漏斗离子反应,错误;B、醋酸是弱酸,不能写成氢离子形式,错误;C、氨水是弱碱溶液,不能写成氢氧根离子形式,错误;D、在NaOH溶液中加入少量Ca(HCO3)2溶液,则碳酸氢钙全部反应,所以对应的离子方程式是Ca2++2HCO3 - +2OH - = CaCO3↓+ CO32- + 2H2O,正确,答案选D。
考点:考查离子方程式书写正误的判断
本题难度:一般
5、选择题 除去下列物质中所混有少量的杂质,指明应加入的试剂,写出有关的离子反应方程式。
(1)Mg粉(Al粉):试剂 离子方程式 ;
(2)FeCl2溶液(FeCl3):试剂 离子方程式 ;
(3)NaHCO3溶液(Na2CO3):试剂 离子方程式 。
参考答案:(1)NaOH溶液 2A
本题解析:
试题分析:(1)利用铝能与NaOH溶液反应的特性,其它金属不可以,所以选的的试剂为NaOH溶液,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑(2)为不引入新的杂质,加入铁粉将FeCl3转化为FeCl2,离子方程式为:2Fe3++Fe=3Fe2+(3)利用Na2CO3可以和CO2反应生成NaHCO3,故选用CO2,离子方程式为:CO2+CO32-+H2O=2HCO3-
考点:物质除杂的试剂选择和离子方程式的书写。
本题难度:一般