微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 Na2O2与水的反应实际是Na2O2+2H2O═2NaOH+H2O2,反应放热,反应放出的热量使部分H2O2受热分2H2O2═2H2O+O2↑.为了测定某过氧化钠固体的纯度,今做如下实验:①称取过氧化钠固体2.00g;②把这些过氧化钠固体放入气密性良好的气体发生装置中;③向过氧化钠中滴加水,用某一量筒排水集气,量筒内液面在112mL处恰好与水槽内液面相平;④将烧瓶中的液体转移到250mL的容量瓶中,洗涤并将洗涤液也转入容量瓶,然后加入蒸馏水,定容,使液面恰好与刻度相切;⑤用移液管移取25.00mL容量瓶中的液体,放入锥形瓶中,用过量的稀硫酸酸化,然后用0.01mol/L的KMnO4溶液去滴定,至终点时用去了24.20mLKMnO4溶液(此时锰全部以Mn2+存在)
(1)有500ml、250ml、150ml的量筒备用,应选用量程为______的量筒
(2)该实验应选用______(填“酸式”或“碱式”)滴定管
(3)在步骤③测量气体体积时,必须待烧瓶和量筒内的气体都冷却到室温时进行,此时量筒内的液面高于水槽中液面(如图),立即读数会使Na2O2的纯度______(填“偏高”“偏低”或“不变”);应进行的操作是______
(4)在步骤④中用到的仪器除了容量瓶外还需要______
(5)在步骤⑤中反应的离子方程式是______判定滴定达到终点的依据是______
(6)该过氧化钠的纯度为______(用百分数表示,保留一位小数;实验中得到的气体体积均看作为标准状况下)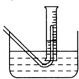
参考答案:(1)用量筒时应选择体积接近的量筒,以减少误差,所以收集11
本题解析:
本题难度:一般
2、实验题 某校化学研究性学习小组设计如下实验方案,测定放置已久的小苏打样品中纯碱的质量分数。
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。实验中加热至恒重的目的是_________________。
(2)方案二:按下图装置进行实验。并回答以下问题:
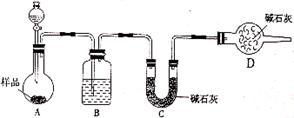
①分液漏斗中应该装___________(填“盐酸”或“稀硫酸”),D装置的作用是_________________________________;
②实验中除称量样品质量外,还需称________装置(用字母表示)前后质量的变化。
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液,过滤洗涤,干燥沉淀,称量固体质量,计算:
①过滤操作中,除了烧杯、漏斗外还用到的玻璃仪器有_____________;
②若加入试剂改为氢氧化钡,已知称得样品9.5g,干燥后的沉淀质量为19.7g,则样品中碳酸钠的质量分数为____________(保留一位小数)。
参考答案:(共12分)
(1)使NaHCO3分解完全
(2
本题解析:
试题分析:(1)小苏打即NaHCO3,加热易分解,故加热至恒重的目的是使NaHCO3分解完全。
(2)①盐酸易挥发,故分液漏斗中应该装稀硫酸,碱石灰能吸收空气中的水蒸气和CO2,故D装置的作用是防止外界CO2、H2O被装置C中的碱石灰吸收。
②A生成CO2气体经B干燥后到C中进行吸收,故还需称C装置前后质量的变化。
(3)①过滤常用的玻璃仪器有烧杯、漏斗和玻璃棒。
②发生反应Na2CO3+Ba(OH)2=BaCO3↓+2NaOH,NaHCO3+Ba(OH)2=BaCO3↓+
本题难度:一般
3、填空题 切开的金属Na暴露在空气中,其变化过程如下:

(1)反应Ⅰ的反应过程与能量变化的关系如下:
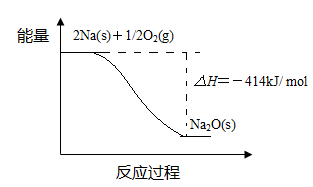
① 反应Ⅰ 是 反应(填“放热”或“吸热”),判断依据是 。
② 1 mol Na(s)全部氧化成Na2O(s)的热化学方程式是 。
(2)反应Ⅱ是Na2O与水的反应,其产物的电子式是?????。
(3)白色粉末为Na2CO3。将其溶于水配制为0.1 mol/L Na2CO3溶液,下列说法正确的是?????(填字母)。
A.升高温度,溶液的pH降低
B.c(OH-)-c (H+)=c (HCO3-)+2 c (H2CO3)
C.加入少量NaOH固体,c (CO32―)与c (Na+)均增大
D.c (Na+) > c (CO32―) > c (HCO3―) > c(OH―) > c (H+)
(4) 钠电池的研究开发在一定程度上可缓和因锂资源短缺引发的电池发展受限问题。
① 钠比锂活泼,用原子结构解释原因_______。
②ZEBRA 电池是一种钠电池,总反应为NiCl2 + 2Na  ?Ni + 2NaCl。其正极反应式是_____。
?Ni + 2NaCl。其正极反应式是_____。
参考答案:(1)①放热????反应物总能量高于生成物总能量
②
本题解析:
试题分析:(1)①由于反应物的总能量比生成物的总能量高,所以发生的反应Ⅰ是放热反应。② 由题目提供的能量关系可得该反应的热化学方程式为:Na(s)+1/4O2(g)=1/2Na2O(s) △H=-207 kJ/ mol。(2)反应Ⅱ是Na2O与水的反应,Na2O与水反应产生NaOH,反应的方程式为Na2O+H2O =2NaOH。NaOH的电子式为: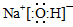 本题难度:一般
本题难度:一般
4、选择题 相同温度下,在甲、乙、丙、丁四个烧杯中分别盛有等体积、等物质的量浓度的NaOH不饱和溶液,分别加入Na、Na2O、Na2O2、NaOH并恢复至原温度,使恰好都形成NaOH饱和溶液,则甲、乙、丙、丁四烧杯中加入的固体质量大小顺序是?? [???? ]
A.丁>丙>乙>甲
B.丁>甲>乙>丙
C.甲=丁>乙=丙
D.丁<丙<乙<甲
参考答案:A
本题解析:
本题难度:一般
5、选择题 一小块钠置于空气中,有下列现象:①变成白色粉末,②变暗,③变成白色固体,④变成液体,上述现象出现的先后顺序是
A.①②③④
B.②③④①
C.②③①④
D.③②④①
参考答案:B
本题解析:
试题分析:现象的本质是发生了什么变化,有什么样的变化就应该有什么样的现象相对应,钠置于空气中发生的变化如下:Na→Na2O→NaOH→Na2CO3·10H2O→Na2CO3,答案选B。
点评:本题考查的是钠的基本性质,比较简单。
本题难度:简单