微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 化学学习小组为测定某补血剂中硫酸亚铁的含量进行了以下探究:
【查阅资料】本品为糖衣片,除去糖衣后显淡蓝绿色,主要成分硫酸亚铁(FeSO4・7H2O)。
【实验步骤】取本品10片,在适当的条件下配成100 mL溶液,分别准确量取20 mL溶液,用下列两种方法进行实验:
方法一:用一定物质的量浓度的酸性高锰酸钾溶液滴定。
方法二:加过量H2O2溶液,然后再加入过量NaOH溶液,得红褐色沉淀,将沉淀过滤并充分加热得红棕色固体,称量该固体的质量。
请回答下列问题:
(1)方法一中,配制一定物质的量浓度的酸性高锰酸钾溶液时,所需要的玻璃仪器除量筒、玻璃棒、胶头滴管、烧杯外还有________。
(2)方法二中,加过量H2O2溶液的目的是________。有的同学认为使用氯气也能达到此目的,和使用氯气相比,用H2O2溶液的好处是________。
(3)在方法一中,若每消耗1 mL酸性高锰酸钾溶液相当于0.152 g FeSO4,则该溶液中高锰酸钾的物质的量浓度是____________。在方法二中,若称得红棕色固体的质量为ag,则每片补血剂含FeSO4______g。
参考答案:(1)容量瓶
(2)使Fe2+完全氧化成Fe3+;无污
本题解析:
本题难度:一般
2、选择题 有Na2CO3、AgNO3、BaCl2、HCl及NH4NO3无标签溶液,为鉴别它们,取四只试管分别装入一种溶液,向上述四只试管中加入少许剩下的一种溶液,下列结论错误的是( )
A.有三只试管出现沉淀时,则后加入的是AgNO3溶液
B.全部若没有什么现象变化时,后加的是NH4NO3溶液
C.一只试管出现气体,两只试管出现沉淀时,最后加入的是HCl溶液
D.若只有两只试管出现沉淀时,则最后加入的可能是BaCl2溶液
参考答案:C
本题解析:
本题难度:简单
3、实验题 过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
I.测定过氧化氢的含量
请填写下列空白:
(1)移取10.00 mL密度为p g/mL的过氧化氢溶液至250 mL_______ (填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25. 00 mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。
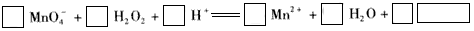
(3)滴定时,将高锰酸钾标准溶液注入_________________ (填“酸式”或“碱式”)滴定管中。 滴定到达终点的现象是____________________________ 。
(4)重复滴定三次,平均耗用cmol/L KMnO4标准溶液VmL,则原过氧化氢溶液中过氧化氢的质量分数为____。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果____________________(填 “偏高”或“偏低”或“不变”)。
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选)
(6)?请将他们的实验方法和实验现象填入下表:
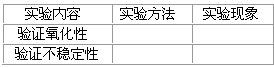
参考答案:(1)容量瓶
(2)2; 5; 6 ;2 ;8 ;5O
本题解析:
本题难度:困难
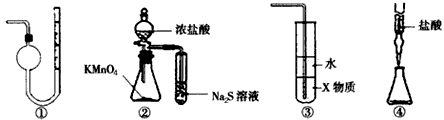
4、选择题 下列装置或操作不能达到实验目的的是
 [???? ]
[???? ]
A.装置①可用于测量气体的体积
B.装置②可用于比较KMnO4、Cl2、S的氧化性
C.装置③中若X为四氯化碳,可用于吸收氨气,并防止倒吸
D.装置④可用于量取15.00 mL盐酸
参考答案:D
本题解析:
本题难度:一般
5、简答题 下列关于实验的叙述中,不正确的是______(填字母).
A.给铜器件镀银时,铜器件连接电源的正极,纯银板连接电源的负极,用AgNO3溶液作为电镀液
B.用金属钠分别与水、乙醇反应,可比较两者中羟基的活泼性
C.除去乙酸乙酯中混有的少量乙酸,先向其中加入适量的无水乙醇,再充分加热
D.向2mL?10%CuSO4溶液中滴入2%的NaOH溶液4~6滴,振荡后加入淀粉的水解液(淀粉和稀硫酸的混合液且加热4~5min)2mL,加热至沸腾,则有红色沉淀出现
E.做甲烷和氯气的取代反应实验的方法是:用排饱和食盐水法在集气瓶中先充入
4
5
体积的氯气和1
5
体积的甲烷气体,用灯光照射瓶中的混合气体.
参考答案:A.镀银,银应作阳极,则纯银板连接电源的正极,故A错误;
本题解析:
本题难度:一般
|
|