��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ͼװ�òⶨˮ���⡢��Ԫ�ص������ȣ��䷽���Ƿֱ�ⶨͨ����ǰ�����ܵ��������U�ιܵ������ʵ����m(H)��m(O)>1��8�����жԵ�����һ�����ԭ��ķ����У�һ���������(����)
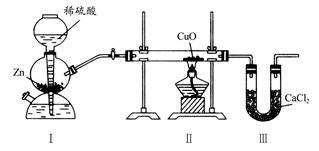
A����װ��֮��ȱ�ٸ���װ��
B����װ�ú�ȱ�ٸ���װ��
C����װ���в���������ˮ����
D��CuOû��ȫ������ԭ
�ο��𰸣�D
�����������H2��ԭCuOʱ��װ�â���CaCl2���յ������ɵ�ˮ����װ�â��в�����ͨH2ǰ���������Ϊ��Ӧʱ����CuO������������������ˮ����Ԫ�ص���������m(ˮ)��m(��)��m(��)����Zn��ϡ���ᷴӦ������H2������[m(ˮ)ƫ��]��װ�â�Ӹ���װ�ã�ʹ����CaCl2���տ����е�ˮ��[m(ˮ)ƫ��]�����в���������ˮ����[m(��)ƫС]��������ɲ��m(H)��m(O)>1��8��H2O�������CuO�Ƿ���ȫ��Ӧ�أ�ֻ��ͨH2ǰ�����ܵ�����������ɵ�ˮ�йء�
�����Ѷȣ�һ��
2��ʵ���� (10��)��ɡ�ұ���͵�ƹ�ҵ������������軯�������ˮ�����к��軯������HCN��CN -�ͽ������ӵ�������M(CN)nm-����ʽ������ˮ�С��ⶨ��ˮ�к��軯���ﺬ����ʵ�鲽�����£�
��ˮ��Ԥ������ˮ���м��������EDTA����pH��2�������¼��������������е�HCN������NaOH��Һ���ա�
�ڵζ���������Һ������pH��11������������ָʾ������AgNO3����Һ�ζ�
Ag++2CN - ="=" [Ag(CN)2] -
�յ�ʱ����Һ�ɻ�ɫ��ɳȺ�ɫ��
��������֪ʶ�ش��������⣺
��1��ˮ��Ԥ������Ŀ����???????????????????????????????��
��2��ˮ��Ԥ������װ������ͼ��ϸ���ܲ�������Һ����Ϊ��??????????????????????��

��3������ƿ������Һ��Ҫ�߳��ܶ࣬��Ŀ����????????????????????????��
��4���������������������Ԥ������ʵ������??????????(�ƫ�ߡ�������Ӱ�족��ƫ�͡�)��
��5��ȷ��ȡij������ˮ100mL������������Ũ��Ϊ0.01000mol��L-1������������Һ�ζ����յ�ʱ������21.00mL����ˮ���к��軯����ĺ���Ϊ?????????????mg��L-1����CN-�ƣ�����������һλС������
�ο��𰸣���1�������軯����ȫ��ת��ΪCN �C
��2����ȫ����H
�����������1�����������Ϣ����ˮԤ������Ŀ���ǽ�������̬���軯����ת��Ϊ���Բⶨ��HCN��
��2��Ϊ�˱�֤���ɵ�HCNȫ�������գ�������Ҫ����NaOH��Һ�С�
��3����������������NaOH��Һ���п��������������Խ���ƿλ�ùҸߡ�
��4�����������������ᣬ������лӷ��ԣ�Ҳ��NaOH��Һ���գ�����������Һ���еζ�ʱ������������Һ���࣬���ƫ�ߡ�
��5������ʵ��ԭ����2HCN��2CN����AgNO3��
m��CN����=0.01000��21��10-3��2��26��103��0.1=109.2mg/L��
�����Ѷȣ�һ��
3��ѡ���� ��ʵ���ҽ��������й����ʵ��Ʊ��У���������ȷ�������Ͽ��С�������ɫ��ѧ˼����ǣ�������
A��C
�ڿ����е�ȼ
COCuO����
CO2?NaOH��Һ
Na2CO3
B��CuHNO3��Һ
Cu��NO3��2��ҺNaOH��Һ
Cu��OH��2
C��Fe??��ȼ
?Fe2O3??H2SO4��Һ
? Fe2��SO4��3��Һ
D��CaO?H2O
??Ca��OH��2��Һ?Na2CO3
?NaOH��Һ
�ο��𰸣�A��̼����ȫȼ�տ�����һ����̼��һ����̼������������ͭ��Ӧ��
���������
�����Ѷȣ���
4��ʵ���� ijͬѧ�������ͼ��ʾװ�ã��г�����ʡ�ԣ�����ϵ��ʵ�飬ʵ��ʱ��ҩƷA��μ��뵽����B�У����������ʵ��ش����⣺
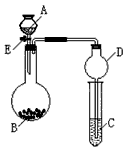
��1����AΪˮ��BΪ�������ƣ�C��ʢ���ữ����FeCl2��Һ����������E��C�е�����Ϊ_________________________�� C�з�����Ӧ�����ӷ���ʽΪ__________________________��
��2����������װ�û�������֤���ʵ����ʣ������֤�������ԣ�KMnO4>Cl2������ȡƯ��Һ����A�м�Ũ���ᣬB�м�___________��Һ�� C�з�����Ӧ�����ӷ���ʽΪ________________________��
��3����������װ�û�������֤SO2�Ļ�ѧ���ʣ�AΪ���ᣬBΪ�������ƹ��壬��ôC��ʢ��__________��Һʱ����֤�仹ԭ�ԣ���C��ʢ��______________��Һʱ����֤��Ư���ԡ�
�ο��𰸣���1����Һ��dz��ɫ��Ϊ���أ���ɫ��4Fe2++O2+4H
���������
�����Ѷȣ�һ��
5��ѡ���� ����ʵ���ܴﵽԤ��Ŀ�ĵ���
���
| ʵ������
| ʵ��Ŀ��
|
A
| �ȼ�������ˮ��Ȼ���ټ������Ը��������Һ
| Ҫ����ϩ���Ƿ���������ױ�
|
B
| ��ʯ���ѽ���ͨ�����Ը������
| ȷ���ѽ����к�����ϩ
|
C
| ������Һ��ϡH2SO4��ϼ��ȣ�������Ƶ�Cu(OH)2����Һ����������
| �������ˮ������л�ԭ��
|
D
| ���Ҵ���Ũ���Ṳ���Ƶõ�����ͨ������KMnO4��Һ��
| ���������к�����ϩ
�ο��𰸣�A
���������A��ȷ���ȼ�������ˮ��ʹ��ϩ�������ӳɴﱥ�ͣ�Ȼ���ټ������Ը��������Һ������Һ��ɫ����˵����ϩ���Ƿ���������ױ���
B������ʯ���ѽ���ͨ�����Ը�����أ���Һ��ɫֻ��˵������̼̼˫�������壬������һ������ϩ��
C�����������ˮ������л�ԭ�ԵIJ�������Ϊ��������Һ��ϡH2SO4��ϼ��ȣ���ȴ���������������������Һ�к����ᣬ������Ƶ�Cu(OH)2����Һ���������ڣ����к�ɫ�������ɣ�����˵������ˮ������л�ԭ�ԡ�
D�������Ҵ���Ũ���Ṳ���Ƶõ��������������Ҵ��������Ҵ�����Ҳ��ʹ����KMnO4��Һ��ɫ����������˵��������ϩ���壻
�����Ѷȣ���
|
��վ�ͷ�QQ: 960335752 - 14613519 - 791315772