��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��ȥ���������������������ʵ���ѡ�Լ�����ȷ���ǣ�������
| ��?�� | ��?�� | ��?��
A
Cl2
HCl
����ʳ��ˮ
B
CO2
HCl
����Na 2CO3��Һ
C
����þ
������
ϡNaOH��Һ
D
FeCl2
FeCl3
����
A��A
B��B
C��C
D��D
�ο��𰸣�A��Cl2�����ڱ���ʳ��ˮ����HCl���ڱ���ʳ��ˮ�����Կ���
���������
�����Ѷȣ�һ��
2��ѡ���� �������dz��õ�ʵ������������ʵ������У���Ҫʹ�ò��������ǣ���������
�ٹ��ˣ�
��ʵ������������
��ϡ��Ũ���
����ʳ������50g������������Ϊ5%���Ȼ�����Һ��
A���ٺ͢�
B���٢ۢ�
C����
D���٢ڢۢ�
�ο��𰸣��ٹ��˲������ò������������ʢ�ѡ��
��ʵ������Ũ�����
���������
�����Ѷȣ���
3������� ��1���� ����������ȼ�� �� ������������ȼ�� �� ��˿��������ȼ�� �� ������������ȼ�ն�����4����ѧ��Ӧ���ԴӲ�ͬ�ĽǶȷ��ࣺ____________��_____________��______________�������ٷ����ࣩ
��2���Ķ������������������ϣ�
����һ��
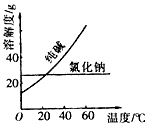
���϶���
|
|
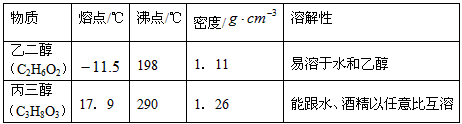
�ش��������⣨����ţ���
A������ B����ȡ�� C�����ܽ⡢�ᾧ�����ˡ��ķ��� D����Һ��
�� ��������Ȼ��ƺʹ���Ļ�����з�����������Ӧ��______________��
�� ���Ҷ����ͱ�������������ѷ�����________________��
�ο��𰸣���1�����Ϸ�Ӧ��������ԭ��Ӧ�������ӷ�Ӧ
��2����C��
���������
�����Ѷȣ�һ��
4��ʵ���� �������Ʊ���Ϊ��ҵ�Σ���Ư�ס���Ƶȷ���Ӧ�ù㷺����ľ̿��Ũ���ᡢˮ��ͭΪԭ�����ɵ�һ��������������Ʒ�Ӧ�Ʊ��������Ƶ�װ������ͼ��ʾ�����ּг�װ���ԣ���
��֪�������£���2NO+Na2O2��2NaNO2??��3NaNO2+3HCl��3NaCl+HNO3+2NO��+H2O��
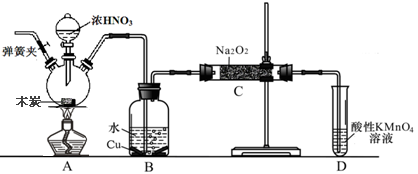
�����������£�NO��NO2�C������MnO4�C��Ӧ����NO3�C��Mn2+
���������գ�
��1��д��Ũ������ľ̿��Ӧ�Ļ�ѧ����ʽ?????????????????????????????????????��
��2��B�й۲쵽����Ҫ������???????????????????????��Dװ�õ�������?????????��
��3������C�в������������Ƶķ�����?????????????????????��
��4��������C�����г�������������и�����̼���ƺ�??????????��Ϊ���������Щ������Ӧ��B��Cװ�ü�����װ��E������E��ע��E��ʢ�ŵ�ҩƷ����??????????��
��5��д������C�������Ƿ�̼���Ƶķ���?????????????????????????????????��
��6����1.56g����������ȫת����Ϊ�������ƣ�������������Ҫľ̿????????g��
�ο��𰸣���1��C+4HNO3(Ũ)=����=CO2+4NO2+2H2O
���������
�����������1��д��Ũ������ľ̿�ڼ��������·���������ԭ��Ӧ�Ļ�ѧ����ʽC+4HNO3(Ũ)=����=CO2+4NO2+2H2O��
��2��A�����ɵĶ�����������B�в���ˮ��Ӧ�����������ᣬ�����ͭ��Ӧ���۲쵽����Ҫ������ͭƬ���ܽ⣬��Һ��Ϊ��ɫ������ɫ�������������һ�������ж���Dװ�õ�����������δ��Ӧ��NO��
��3������C�в������������Ƶķ�����ȡ��������ϡ���ᣬ������ɫ���壬����������Ϊ����ɫ��
��4��������C�����г�������������и�����̼���ƺ��������ƣ�������������ˮ�����������ɣ�Ϊ���������Щ������Ӧ��B��Cװ�ü����Ӹ���װ��E��ҩƷ���Ƽ�ʯ�ҷ��ڸ�����С�
��5������̼����ķ�����ȡ�����������Ը��������Һ������ʹ����ʯ��ˮ����ǵ��������������̼���ơ�
��6����1.56g����������0.02mol����ȫת����Ϊ�������ƣ����ݢ�2NO+Na2O2��2NaNO2������NaNO2 0.04mol��C+4HNO3(Ũ)=CO2+4NO2+2H2O��3NO2+2H2O=2HNO3 + NO +H2O���ó���ϵʽ1.5C---2NaNO2,�����̼�����ʵ���Ϊ0.03mol��������������Ҫľ̿0.36g��
�����Ѷȣ�һ��
5��ѡ���� ijʵ��̽��С��Ϊ����CO��CO2���������ͼ��ʾװ�ã�����������ȷ����
 [???? ]
[???? ]
A����ƿ����ʢ����Һ�dz���ʯ��ˮ����ƿ����ʢ����Һ��Ũ����
B����ƿ����ʢ����Һ�DZ���̼������Һ����ƿ����ʢ����Һ��Ũ����
C������A������B�رգ����Է���õ������CO������B������A�رգ����Եõ������CO2
D��ʵ�����о������ַ�����Էֱ�õ�������CO��CO2
�ο��𰸣�C
���������
�����Ѷȣ�һ��