��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���µķ���ʽ��ȷ���ǣ�������
A��Fe+Cl2
?��ȼ?
.
?
FeCl2
B��Na2SiO3+2HCl=2NaCl+H2SiO3�����壩
C��4HNO3��Ũ��+Cu=Cu��NO3��2+2NO��+2H2O
D��4H2SO4��Ũ��+Fe=FeSO4+4H2��
�ο��𰸣�B
���������
�����Ѷȣ���
2��ѡ���� �����йػ�ѧ�����ʾ��ȷ���ǣ�??��
A��������(C6H12O6)�Ľṹ��ʽ��CH2O
B��Cl���Ľṹʾ��ͼ��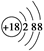
C��������Ϊ8��̼ԭ�ӣ�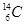
D��NaCl�ĵ���ʽ��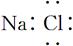
�ο��𰸣�C
���������A������ǵĽṹ��ʽΪCH2(CHOH)4OHCHO��B�Cl���Ľṹʾ��ͼΪ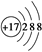 ��D�NaCl�ĵ���ʽΪ ��D�NaCl�ĵ���ʽΪ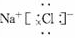 ��C�� ��C��
�����Ѷȣ���
3������� ������Na2CO3?����;�У�����������Na2CO3��ʲô���ʣ�
��1������ϴȥijЩ���ʱ��������______
��2���Ŵ������Ƽ��У���Na2CO3��Ca��OH��2��Ӧ���ռ�û�ѧ����ʽ��ʾ��______��
�ο��𰸣���1�����۵���Ҫ�ɷ�Ϊ��֬���ڼ�������������ˮ�⣬��Na2
���������
�����Ѷȣ���
4��ѡ���� ��֪��Ӧ����Cl2+2KBr====2KCl+Br2����KClO3+6HCl(Ũ)====3Cl2��+KCl+3H2O����2KBrO3+Cl2====Br2+2KClO3������˵����ȷ���ǡ�(����)
A������3����Ӧ�����û���Ӧ
B����������ǿ������˳��ΪKBrO3>KClO3>Cl2>Br2
C����Ӧ�������õ�6��72 L Cl2(��״��)�������ת�Ƹ���Ϊ3��01��1023
D������1 mol�������μӷ�Ӧ�õ����ӵ����ʵ���Ϊ2 mol
�ο��𰸣�B
���������
��������������������е��ʵ���Ӧ��û�е��ʣ����Բ����û���Ӧ����A����Cl2+2KBr====2KCl+Br2���������������������������壬���������������Դ����壬��KClO3+6HCl====3Cl2+KCl+3H2O��������������أ���������������������ص������Դ�����������2KBrO3+Cl2====Br2+2KClO3��������������أ���������������أ���������ص������Դ�������أ���֮��������ǿ��˳����KBrO3>KClO3>Cl2>Br2����B��ȷ����Ӧ�������õ�6��72 L Cl2(��״��)�������ת�Ƹ���= ��1��(5-0)��NA=9��03��1023����C����Ӧ2KBrO3+Cl2====Br2+2KClO3��1 mol�������μӷ�Ӧ�õ����ӵ����ʵ���Ϊ1 mol��(5-0)="5" mol����D���� ��1��(5-0)��NA=9��03��1023����C����Ӧ2KBrO3+Cl2====Br2+2KClO3��1 mol�������μӷ�Ӧ�õ����ӵ����ʵ���Ϊ1 mol��(5-0)="5" mol����D����
���㣺������ԭ��Ӧ
�����Ѷȣ�һ��
5��ѡ���� ��֪�ס������ʵ�������������Һ�ܶȵĹ�ϵ���±���ʾ��
���ʵ���������
| ����Һ�ܶȨug��cm-3
| ����Һ�ܶȨug��cm-3
| 1%
| 0.95
| 1.02
| 5%
| 0.92
| 1.04
| 9%
| 0.90
| 1.07
�����ʵ�1%����Һ��9%����Һ�������ϣ������ʵ�1%����Һ��9%����Һ�������ϣ����������У���ȷ����
A����Ϻס�����Һ�����ʵ���������������5%
B����Ϻ�����Һ�����ʵ�������������5%������Һ�����ʵ���������С��5%
C����Ϻ���Һ�����ʵ�������������5%������Һ�����ʵ���������С��5%
D����Ϻס�����Һ�����ʵ���������������5%
�ο��𰸣�B
���������
���⿼������������������Һ�ܶȵĹ�ϵ��������Һ���ܶȴ�С���������ֲ�ͬŨ�ȵ���Һ��������ϣ������������������ߵ�ƽ��ֵ������ǵ������ϣ����ܶȴ���1ʱ�������������������ߵ�ƽ��ֵ�������ܶ�С��1ʱ������������С�����ߵ�ƽ��ֵ���ʱ���ֻ��Cѡ��������⡣
�����Ѷȣ�һ��
|
|
��վ�ͷ�QQ: 960335752 - 14613519 - 791315772