��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��֪H��(aq)��OH��(aq)=H2O(l)? ��H����57.3 kJ��mol��1���ش��й��кͷ�Ӧ�����⡣
��1����0.1 mol Ba(OH)2���ϡ��Һ������ϡ���ᷴӦ���ܷų�________kJ������
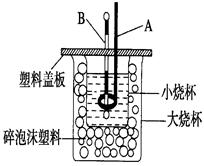
��2����ͼװ��������A��������??????????????????????????????????????????������ĭ���ϵ�������???????????????????????????????????????????��
��3����ͨ��ʵ��ⶨ�к��ȵĦ�H�������������ڣ�57.3 kJ��mol��1����ԭ�������????????????
?????????????????????????????????????????????????????????????????????��
��4������ͬŨ�Ⱥ�����İ�ˮ(NH3��H2O)����NaOH��Һ��������ʵ�飬��õ��к��ȵ���ֵ��????????(�ƫ����ƫС��������Ӱ�족)��
�ο��𰸣���1��11.46
��2�����β�������������ȣ���������
���������
�����������1����H����aq��+OH����aq���TH2O��l����H=-57.3kJ��mol��1��֪����1molH2O�ų�����Ϊ57.3kJ����0.1mol Ba(OH)2���ϡ��Һ������ϡ���ᷴӦ�ɵ�0.2molH2O�����Էų�������Ϊ57.3kJ��0.2=11.46kJ����Ϊ��11.46��
��2������A�������ǻ��β�����������к��Ȳⶨʵ��ɰܵĹؼ��DZ��¹�������С�ձ�֮����������ĭ���ϵ������ǣ����β�������������ȣ���������ɢʧ����Ϊ�����β�������������ȣ���������ɢʧ��
��3��
�����Ѷȣ���
2��ѡ���� ����˵���д������
A���ⶨ�к��ȵ�ʵ����ÿ��ʵ����Ҫ�ⶨ�����¶�����
B����ѧ���Ķ��Ѻ��γ��ǻ�ѧ��Ӧ�������仯����Ҫԭ��
C���������ȶ������Ļ�ѧ��Ӧ�������ȷ�Ӧ
D����Ӧ��������������������������Դ�С�����˷�Ӧ�Ƿ��Ȼ�������
�ο��𰸣�C
���������
�𰸣�C
C������ȷ������ֻ��Ϊ��Ӧ��Ļ�ѧ������Ӧ���Ȼ��Ƿ��Ⱦ����ڲ�Ӧ��Ļ�ѧ�������յ��������γ����������ų���������Դ�С��
A����ȷ����⼸�Σ�Ϊ�˼�С��
B����ȷ����Ӧ���Ȼ��Ƿ��Ⱦ����ڲ�Ӧ��Ļ�ѧ�������յ��������γ����������ų���������Դ�С����ѧ���Ķ��Ѻ��γ��ǻ�ѧ��Ӧ�������仯����Ҫԭ��
D����ȷ���������仯�ĽǶȣ���Ӧ��������������������������Դ�С�����˷�Ӧ�Ƿ��Ȼ������ȡ�
�����Ѷȣ�һ��
3��ѡ���� �к��Ȳⶨʵ���У���50mL0.50mol/L�����50mL0.55mol/LNaOH����ʵ�飬����˵��������ǣ�????��
A������60mL 0.50mol/L�����50mL 0.55 mol/L NaOH��Һ���з�Ӧ��������к�����ֵ��ԭ����ͬ
B����50mL0.50mol/L�����50mL0.55mol/LNaOH����ʵ�����50mL0.50mol/L����50mL0.50mol/LNaOH��õ���ֵȷ
C�������ʱ����Ͳ��NaOH��ҺӦ��������С�ձ��У������ò���������
D��װ���еĴ�С�ձ�֮����������ĭ���ϵ������DZ��¸��ȡ�����������ʧ
�ο��𰸣�C
���������
����������к���ָ��ϡ��Һ�У��������кͷ�Ӧ����1 molˮʱ�ķ�Ӧ�Ƚ����к��ȡ�Aѡ���ȷ��Bѡ�����������ʹ��Ӧ����ȫ����ȷ��Cѡ����������ҺʱӦ���ټ��롣Dѡ���ȷ��
�����Ѷȣ�һ��
4��ѡ���� ��������������������������������Ľ��죬�о���ѧ��Ӧ���������仯�Ժ������ó�����Դ�Ϳ�������Դ����ʮ����Ҫ�����塣����˵���в���ȷ����
A���κλ�ѧ��Ӧ�������������ı仯
B����ѧ��Ӧ�е������仯������Ϊ�����ı仯
C����Ӧ������������������������������Ӧ�ͷ�����
D������ѧ���γ�ʱ�ͷŵ�����С�ھɻ�ѧ�����ƻ�ʱ��Ҫ���յ���������Ӧ��������
�ο��𰸣�B
���������
�����������ѧ��Ӧ��ʵ���Ǿɼ������¼��γɣ��ϼ���Ҫ�����������ɼ��ͷ�����������κλ�ѧ��Ӧ�����������仯������ѧ���γ�ʱ�ͷŵ�����С�ھɻ�ѧ�����ƻ�ʱ��Ҫ���յ���������Ӧ������������A��D��ȷ����ѧ��Ӧ�������仯�������⣬���ɱ���Ϊ���ܡ����ܵȣ�B����Ӧ������������������������������Ӧ�ͷ�������C��ȷ��
�����Ѷȣ���
5��ѡ���� ����ͼʾ���Ӧ�������������
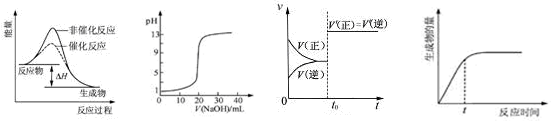
��???????????????��????????????????��???????????????????��
A��ͼ�ٱ�ʾij���ȷ�Ӧ�ֱ����С�����������·�Ӧ�����е������仯
B��ͼ�ڱ�ʾ0.1000 mol��L��1NaOH��Һ�ζ�20.00mL 0.1000 mol��L��1HCl��Һ���õ��ĵζ�����
C��ͼ�۱�ʾ�Ѵ�ƽ���ij��Ӧ����t0ʱ�ı�ijһ������Ӧ������ʱ��仯����ı������һ���Ǽ������
D��ͼ�ܱ�ʾij���淴Ӧ����������淴Ӧʱ��仯�����ߣ���ͼ֪tʱ��Ӧ��ת�������
�ο��𰸣�B
���������ͼ���з�Ӧ�����������������������������Ƿ��ȷ�Ӧ������ȷ��ͼ���иı��������һ���Ǵ���������÷�Ӧ�Ƿ�Ӧǰ���������ķ�Ӧ��������ѹǿ����Ӧ��������ƽ�ⲻ�ƶ�������ͼ��ܿ�֪��tʱ�̷�Ӧ��û�дﵽ��ѧƽ��״̬����˸�ʱ��ת���ʲ������ģ�������ȷ�Ĵ���B��
�����Ѷȣ�һ��