微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 绿矾晶体(FeSO4・7H2O,M=278g/mol)是治疗缺铁性贫血药品的重要成分。实验室利用硫酸厂的烧渣(主要成分为Fe2O3及少量FeS、SiO2),制备绿矾的过程如下:
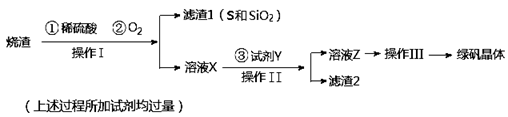
试回答:
(1)操作I为?????????????(填写操作名称)。
(2)试剂Y与溶液X反应的离子方程式为??????????????????????????????????。
(3)操作III的顺序依次为:?????????????、冷却结晶、过滤、 ??????????、干燥。
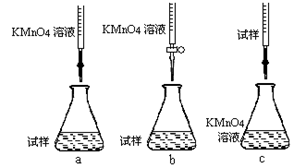
(4)某同学用酸性KMnO4溶液测定绿矾产品中Fe2+含量:
a.称取11.5g绿矾产品,溶解,配制成1000mL溶液;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。①步骤a配制溶液时需要的玻璃仪器除玻璃棒、量筒、烧杯、胶头滴管外,还需????????????????。②该同学设计的下列滴定方式,最合理的是??????(夹持部分略去)(填字母序号)。
③滴定时发生反应的离子方程式为: 。
④判断此滴定实验达到终点的方法是?????????????;若在滴定终点读取滴定管刻度时,俯视KMnO4溶液液面,其它操作均正确,则使测定结果????????(填“偏高”“偏低”“无影响”)。
⑤计算上述样品中FeSO4・7H2O的质量分数为????????????????。
参考答案:(1)过滤(1分)?(2)Fe+2Fe3+=3Fe2+(1分
本题解析:
试题分析:(1)由于烧渣中含有与稀硫酸以及氧气不反应的二氧化硅,所以操作I是过滤。
(2)由于滤液中含有铁离子以及过量的稀硫酸。而最终制备的是绿矾,所以需要将溶液中的铁离子还原为亚铁离子,因此试剂Y是铁粉,所以有关反应的离子方程式为Fe+2Fe3+=3Fe2+、Fe+2H+=Fe2++H2↑。
(3)操作Ⅲ的目的是得到绿矾晶体,所以正确的操作应该是蒸发浓缩、冷却结晶、过滤、洗涤然后干燥即可。
(4)①准确配制一定物质的量浓度溶液的主要仪器是容量瓶,所以步骤a配制溶液时需要的玻璃仪器除玻璃棒、量筒、烧杯、胶头滴管外,还需1000ml容量瓶。
②由于酸性高锰酸钾溶液具有强氧化性与酸性,因此应该放在酸式滴定管中,答案选b。
③酸性高锰酸钾溶液具有强氧化性,能把亚铁离子氧化生成铁离子,而自身被还原为Mn2+,因此该反应的离子方程式为5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O。
④由于酸性高锰酸钾溶液显紫红色,所以判断此滴定实验达到终点的方法是滴加最后一滴KMnO4溶液时,溶液变成紫色且半分钟内不再褪色;由于滴定管的刻度自上而下逐渐增大,所以若在滴定终点读取滴定管刻度时,俯视KMnO4溶液液面,则读数值偏小。如果其它操作均正确,则使测定结果偏低。
⑤根据反应式可知,反应中消耗亚铁离子的物质的量=0.01000mol/L×0.02000L×5=0.001mol,则原样品中绿矾的物质的量=0.001mol×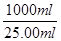 =0.04mol,质量=0.04mol×278g/mol=11.12g,所以上述样品中FeSO4・7H2O的质量分数为
=0.04mol,质量=0.04mol×278g/mol=11.12g,所以上述样品中FeSO4・7H2O的质量分数为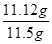 ×100%=96.7%。
×100%=96.7%。
本题难度:一般
2、选择题 下列实验操作与预期实验目的或实验结论不一致的是
选项
| 实验操作及现象
| 实验目的或结论
|
A
| 将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色
| 可证明氧化性:H2O2比Fe3+强
|
B
| 在0.1 mol・L-1的NaHCO3溶液中,加2滴酚酞显浅红色,微热,溶液颜色加深
| 验证盐类水解反应是吸热反应
|
C
| 将一定量的NaNO3和KCl的混合液加热并
浓缩至有晶体析出时,趁热过滤
| 得到NaCl晶体
|
D
| 苯酚钠溶液中通入足量二氧化碳产生浑浊
| 苯酚的酸性弱于碳酸
?
参考答案:A
本题解析:
试题分析:A、硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,NO3?、H+具有强氧化性,能把Fe2+氧化为Fe3+,不能证明H2O2的氧化性大于Fe3+,错误;B、微热,溶液颜色加深,c(OH-)增大,说明加热促进HCO3?的水解,可证明盐类水解反应是吸热反应,正确;C、因为KNO3、KCl、NaNO3的溶解度都随温度升高而增大,NaCl受温度影响不大,正确;D项利用强酸制弱酸原理,正确。
本题难度:一般
3、填空题 (14分)废旧碱性锌锰干电池内部的黑色物质A主要含有MnO2、NH4CI、ZnCI2,还有少量的FeCI2和炭粉,用A制备高纯MnCO3,的流程图如下。
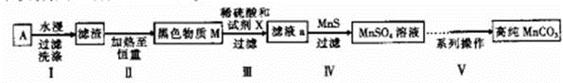
(1)碱性锌锰干电池的负极材料是_________(填化学式)。
(2)第Ⅱ步操作的目的是________________________。
(3)第Ⅳ步操作是对滤液a进行深度除杂,除去Zn2+的离子方程式为____________________。
(已知:Ksp(MnS)=2.5×10-13,Ksp(ZnS)=1.6×10-24)?
(4)为选择试剂X,在相同条件下,分别用5 g黑色物质M进行制备MnSO3的实验,得到数据如右表:

①试剂x的最佳选择是_________。
②第Ⅲ步中用选出的最佳试剂X与M的主要成分反应的化学方程式为_________。
(5)已知:MnCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH为7.7。请补充完成以下操作:
第Ⅴ步系列操作可按一下流程进行:请补充完成操作:(第Ⅴ步系列操作中可供选用的试剂: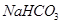 、乙醇) 、乙醇)
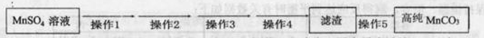
操作1:___________________;操作2:过滤,用少量水洗涤2~3次
操作3:检测滤液,表明SO42-已除干净; 操作4:___________________;
操作5:低温烘干。
(6)操作1可能发生反应的离子方程式????????????????????????????????
参考答案:(14分,每空2分)
(1)Zn
(2)除去碳粉
本题解析:
试题分析:(1) 碱性锌锰干电池中,锌比锰活泼,所以负极材料是Zn;
(2)第I步操作水浸后,溶于水的NH4CI、ZnCI2可除去,而碳粉不溶于水,所以第Ⅱ步操作的目的是除去碳粉;
(3)第Ⅳ步操作中加入MnS目的是利用沉淀的转化除去Zn2+,使MnS转化为更难溶的ZnS,离子方程式为Zn2++MnS=ZnS+Mn2+
(4)①根据表中数据选择30%的过氧化氢得到的MnSO4的质量最多,所以选择30%的过氧化氢;
②根据表可知,过氧化氢是把二氧化锰转化为硫酸锰,本身被氧化为氧气,化学方程式为H2O2+MnO2+H2SO4=MnSO4+2H2O+O2↑
(5)最终产物是碳酸锰,所以第一步应加入NaHCO3,调节pH值使之小于7.7,防止氢氧化锰生成;MnCO3潮湿时易被空气氧化,所以水洗完后再用用少量无水乙醇洗涤2~3次以除去碳酸锰表面的水分;
(6)操作1目的是生成碳酸锰的沉淀,所以可能发生反应的离子方程式Mn2++2 HCO3-= MnCO3↓+H2O+CO2↑
本题难度:困难
4、选择题 除去括号内杂质所用试剂和方法,正确的是
A.A
B.B
C.C
D.D
参考答案:D
本题解析:分析:A、互不相溶的液体可以采用分液的方法分离;
B、乙烯能被高锰酸钾氧化为二氧化碳;
C、乙酸乙酯和水溶液互不相溶,可以采用分液法来分离;
D、互溶、沸点相差较大的液体之间可以采用蒸馏法分离.
解答:A、乙酸和氢氧化钠反应生成乙酸钠溶液和乙醇是互溶的,不能用分液的办法分离,故A错误;
B、乙烯可以被高锰酸钾氧化为二氧化碳气体,除掉了乙烯,又在乙烷中引入了二氧化碳杂质,故B错误;
C、乙酸和碳酸钠可以反应生成醋酸钠的水溶液,乙酸乙酯和醋酸钠溶液互不相溶,可以采用分液法来分离,故C错误;
D、生石灰可以和水发生反应生成氢氧化钙溶液,可以采用蒸馏的方法实现氢氧化钙和乙醇混合溶液的分离,故D正确.
故选D.
点评:本题考查除杂,注意物质的分离与除杂是考试的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.
本题难度:简单
5、实验题 PCl3可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
?
| 熔点/℃
| 沸点/℃
| 密度/g・mL-1
| 其他
| 黄磷
| 44.1
| 280.5
| 1.82
| 2P(过量)+3Cl2 2PCl3;2P+5Cl2 2PCl3;2P+5Cl2 2PCl5 2PCl5
| PCl3
| ―112
| 75.5
| 1.574
| 遇水生成H3PO3和HCl,遇O2生成POCl3
| POCl3
| 2
| 105.3
| 1.675
| 遇水生成H3PO4和HCl,能溶于PCl3
?
(一)制备:RU 图是实验室制备PCl3的装置(部分仪器已省略)
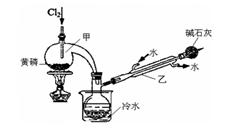
(1)仪器乙的名称____________。
(2)实验室用漂白粉加浓盐酸制备Cl2的化学方程式:_______________________ 。
(3)碱石灰的作用是____________________。
(4)向仪器甲中通入干燥Cl2之前,应先通入一 段时间的CO2,其目的是____________________。
(二)提纯:
(5)粗产品中常含有POCl3、PCl5等。加入黄磷加热除去PCl5后,通过_________________(填实验操作名称),即可得到PCl3的纯品。
(三)分析:
测定产品中PCl3纯度的方法如下:迅速称取4.200 g产品,水解完全后配成500mL溶液,取出25.00mL加入过量的0.1000 mol/L 20.00? mL 碘溶液,充分反应后再用0.1000 mol/L? Na2S2O3溶液滴定过量的碘,终点时消耗10.00? mL Na2S2O3溶液。
已知:H3PO3+H2O+I2=H3PO4+2HI;I2+2Na2S2O3=2NaI+Na2S4O6;假设测定过程中没有其他反应。
(6)根据上述数据,该产品中PCl3的质量分数为____________________ 。若滴定终点时俯视读数,则PCl3的质量分数_______(偏大、偏小、或无影响)
参考答案:(1)冷凝管??(2)Ca(ClO)2+4HCl = CaC
本题解析:
试题分析:(1)仪器乙名称为:冷凝管;(2)实验室制备氯气用漂白粉和浓盐酸反应生成氯化钙、氯气和水,反应的化学方程式为Ca(ClO)2+4HCl = CaCl2+2H2O +2Cl2↑;(3)氯气有毒,污染空气,碱石灰吸收多余氯气防止污染空气,防止空气中的水蒸气进入影响产品纯度;(4)根据题给信息知,PCl3遇O2会生成POCl3,遇水生成H3PO3和HCl,通入一段时间的CO2可以排尽装置中的空气,防止生成的PCl3与空气中的O2和水反应;(5) 由信息可知,POCl3与PCl3都是液体,沸点相差较大,故可以用蒸馏的方法进行分离;(6)H3PO3+H2O+I2=H3PO4+2HI;I2+2Na2S2O3=2NaI+Na2S4O6,依据化学方程式可知H3PO3物质的量和PCl3的物质的量相同,和25ml H3PO3溶液反应的碘单质物质的量为(0.1000 mol/L×0.020L ―1/2×0.1000 mol/L×0.010L)=0.0015mol,500ml溶液中PCl3的物质的量=H3PO3物质的量=碘单质物质的量为0.0015mol×20=0.03mol,PCl3质量为4.125g,该产品中PCl3的质量分数为4.125/4.20×100%=98.21%;若滴定终点时俯视读数,所读Na2S2O3溶液的体积偏小,计算剩余的碘偏小,则PCl3的质量分数偏大。
本题难度:困难
|
|