微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知ag气体X2中含有b个X原子,那么cg该气体在0℃、1.01×105Pa条件下的体积是(NA表示阿伏加德罗常数的值) [???? ]
A.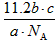 L
L
B.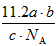 L
L
C.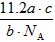 L
L
D.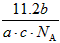 L
L
参考答案:A
本题解析:
本题难度:简单
2、选择题 在MgCl2、KCl、K2SO4三种盐的混合溶液中,若K+、Cl-各1.5mol,Mg2+为0.5mol,则SO42-的物质的量是
A.0.25 mol
B.0.5mol
C.0.75mol
D.0.75mol
参考答案:B
本题解析:
试题分析:根据电荷守恒定律,则n(K+)+2n(Mg2+)=n(Cl-)+2n(SO42-),将数据代入,解得n(SO42-)=0.5mol,答案选B。
考点:考查电荷守恒规律的应用
本题难度:一般
3、选择题 下列叙述错误的是( )
A.物质的量是国际单位制中七个基本物理量之一
B.0.016kg16O含有约6.02×1023个氧原子
C.一定温度、压强下,气体体积由其分子的数目决定
D.1mol氧的质量为16g
参考答案:D
本题解析:
本题难度:简单
4、简答题 常温下,将40克7%的NaCl溶液和60克12%的NaCl溶液混合,得到密度为1.17g/cm的混合溶液,计算:
(1)该混合溶液中溶质的质量分数?
(2)该混合溶液中溶质的物质的量浓度?
参考答案:(1)混合后溶液中NaCl总质量为:40g×7%+60g×1
本题解析:
本题难度:一般
5、选择题 用NA表示阿佛加德罗常数,下列说法正确的是?????(?????)

A.22.4L H2的物质的量约为1mol
B.1 L 1mol/L的MgCl2溶液中Cl-的物质的量浓度为 2mol/L
C.标准状况下,11.2L H2O的物质的量约为1 mol
D.0.1mol铁与足量的盐酸完全反应,铁失去的电子数为0.3NA
参考答案:B
本题解析:A错误,没有表明氢气所处的状态是否是标准状态,无法计算。
B正确。
C错误,标准状态下的水是非气体状态,无法计算。
D错误,铁与盐酸反应生成+2价亚铁离子,0.1mol铁只失去0.2mol电子,数目为0.2NA
本题难度:一般