微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 化学工业是国民经济的支柱产业,下列生产过程中不涉及氧化还原反应的是
A.氮肥厂用氮气和氢气合成氨气
B.硝酸厂用氨氧化法制硝酸
C.从海水中提溴
D.纯碱厂用NaCl、NH3、CO2等制纯碱
参考答案:D
本题解析:
试题分析:A.N2+3H2 2NH3,反应前后元素的化合价发生了变化,是氧化还原反应。错误。B.4NH3+5O2
2NH3,反应前后元素的化合价发生了变化,是氧化还原反应。错误。B.4NH3+5O2 本题难度:一般
本题难度:一般
2、选择题 下列有关物质组成与结构表示方法不正确的是
A.HClO 电子式: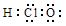
B.CH4比例模型:
C.乙炔结构简式:HC≡CH
D.质子数55,中子数82的原子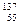 Cs
Cs
参考答案:A
本题解析:略
本题难度:简单
3、简答题 中学化学常见的物质A、B、C、D之间存在如下转化关系:A+B→C+D+H2O(没有配平).请按要求填空:
(1)若A为短周期元素组成的黑色固体单质,与B的浓溶液共热时,产生C、D两种气体.C、D两种气体均能使澄清石灰水变浑浊,则该反应的化学方程式是:______,鉴别这两种气体不能选用的试剂是______
a.BaCl2溶液??b.KMnO4溶液??c.品红溶液?? d.酸化的Ba(NO3)2溶液
向500mL2mol/L的NaOH溶液中通入0.8mol无色无味的C气体,恰好完全反应,该反应的化学方程式是______.此时溶液中的离子按照浓度由大到小排列的顺序是______.
(2)若A为红色金属单质,与适量B的溶液在常温下恰好完全反应,生成的无色气体C遇空气迅速变成经棕色.若被还原的B物质的量为2mol时,产生C气体的体积是______?L(标况).将生成的红棕色气体通入一个烧瓶里,塞紧瓶塞后,将烧瓶浸入冰水中,烧瓶中气体的颜色变浅,请用化学方程式和必要的文字解释颜色变化的原因______.
(3)若A在水中的溶解度随温度的升高而降低;B为短周期非金属单质;D是漂白粉的成分之一.C发生水解反应的离子方程式是______
(4)若A为五核10电子的阳离子与单核18电子的阴离子构成的无色晶体,受热易分解,分解后生成两种极易溶于水的气体.检验A中阴离子的方法是______(简述操作过程及结论).
参考答案:(1)C、D两种气体均能使澄清石灰水变浑浊,能使澄清石灰水变
本题解析:
本题难度:一般
4、选择题 下列是某学生自己总结的一些规律,其中正确的是?
A.氧化物不可能是还原产物,只可能是氧化产物
B.有些化学反应不属于化合、分解、置换、复分解中的任何一种反应
C.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
D.饱和溶液一定比不饱和溶液的浓度大
参考答案:B
本题解析:选项A不正确,氧化产物也可能是还原产物,例如硝酸钡还原生成NO2或NO等;选项C不正确,例如NO2和N2O4中氮元素的化合价都是+4价;饱和溶液的浓度不一定大于不不饱和溶液的浓度,选项D不正确,因此正确的答案选B。
本题难度:一般
5、填空题 (8分)某氮肥厂氨氮废水中氮元素多以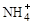 和NH3・H2O的形式存在,该废水的处理流程如下:
和NH3・H2O的形式存在,该废水的处理流程如下:
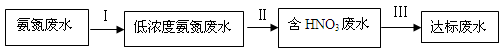
(1)过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30 ℃,通空气将氨赶出并回收。用离子方程式表示加NaOH溶液的作用: 。
(2)过程Ⅱ:在微生物作用的条件下,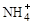 经过两步反应被氧化成
经过两步反应被氧化成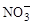 。其中第一步反应的能量变化示意图如下:
。其中第一步反应的能量变化示意图如下:

第一步反应是 反应(选填“放热”或“吸热”),判断依据是
(3)过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32 g CH3OH转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比是 。
参考答案:(1) NH4++OH- 本题解析:
本题解析:
试题分析:(1)过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30 ℃,通空气将氨赶出并回收。用离子方程式表示加NaOH溶液的作用是H4++OH-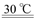 NH3↑+H2O;(2)根据图示可知:反应物的能量高三生成物的能量,所以当反应发生时多余的能量就释放出来,因此第一步反应是放热反应;(3)过程Ⅲ:一定条件下,向废水中加入CH3OH,甲醇在反应中失去电子,作还原剂,而硝酸在反应中得到电子,作氧化剂,甲醇将HNO3还原成N2。若该反应消耗32 g CH3OH转移6 mol电子,每1mol的稀释在反应中得到5mol的电子。根据氧化还原反应中电子转移的数目相等可得:参加反应的还原剂和氧化剂的物质的量之比是5∶6。
NH3↑+H2O;(2)根据图示可知:反应物的能量高三生成物的能量,所以当反应发生时多余的能量就释放出来,因此第一步反应是放热反应;(3)过程Ⅲ:一定条件下,向废水中加入CH3OH,甲醇在反应中失去电子,作还原剂,而硝酸在反应中得到电子,作氧化剂,甲醇将HNO3还原成N2。若该反应消耗32 g CH3OH转移6 mol电子,每1mol的稀释在反应中得到5mol的电子。根据氧化还原反应中电子转移的数目相等可得:参加反应的还原剂和氧化剂的物质的量之比是5∶6。
考点:考查离子方程式的书写、反应热与物质能量的关系、氧化还原反应中的概念和电子转移的关系的知识。
本题难度:一般