微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 设NA为阿伏伽德罗常数的数值,则下列说法中正确的是
①2.24L氨气含有NA个电子,②1.4g乙烯与丙烯的混合气体含有NA个碳原子,③精炼铜,?若阳极失去2NA个电子,则阴极增重64g,④标准状况下,22.4L空气含有NA个分子,⑤过氧化钠与水反应,若电子转移4NA,则产生的氧气为32 g,⑥将1L 2mol/L 的FeCl3溶液加入到沸水中,加热使之完全反应,所得氢氧化铁胶体粒子数为2NA,⑦在1L 0.1mol/L的碳酸钠溶液中,阴离子总数大于0.1NA
A.②③④⑦
B.①③④⑦
C.②③④⑤⑦
D.②④⑤⑦
参考答案:A
本题解析:①不正确,因为不一定是在标准状况下;乙烯和丙烯的最简式相同,都是CH2,所以1.4g含有0.1mol碳原子,②正确;根据电荷守恒可知,③正确;根据阿伏加德罗定律可知,④正确;过氧化钠中氧元素是-1价的,所以如果转移4Na个电子,则生成氧气2mol,质量是64g,⑤不正确;生成氢氧化铁胶体的反应是可逆反应,转化率达不到100%,⑥不正确;根据碳酸钠的水解方程式CO32-+H2O 本题难度:一般
本题难度:一般
2、填空题 (9分) 向浓度相等、体积均为50 mL的A、B两份KOH溶液中,分别通入一定量的SO2气体后,再稀释到100 mL。
(1)在KOH溶液中通入一定量的SO2气体后,溶液中溶质的组成可能是:
① ; ② ;
③ ; ④ 。
(2)在稀释后的溶液中逐滴加入0.1 mol/L的盐酸,产生SO2的体积(标准状况)与所加盐酸的体积关系如下图所示。
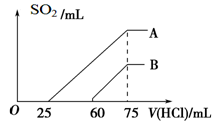
①A曲线表明,原溶液通入SO2气体后,所得溶质与盐酸反应产生SO2的最大体积是____mL(标准状况)。
②B曲线表明,原溶液通入SO2气体后,所得溶液中溶质的化学式为_________________。
③原KOH溶液的物质的量浓度为________ ____。
参考答案:(9分)
(1)① KOH、K2SO3&#
本题解析:
试题分析:(1)二氧化硫与氢氧化钾溶液反应时,若二氧化硫少量,与氢氧化钾恰好反应则生成亚硫酸钾,若二氧化硫过量与氢氧化钾恰好完全反应,则生成亚硫酸氢钾,所以二氧化硫与氢氧化钾溶液反应得到的溶液中溶质可能有四种可能:① KOH、K2SO3;②K2SO3;③ K2SO3、KHSO3; ④KHSO3;
(2)①因为亚硫酸根离子与盐酸反应生成亚硫酸氢根离子消耗盐酸的体积与亚硫酸氢根离子生成二氧化硫消耗盐酸的体积相等。A曲线开始无气体产生,且生成气体消耗的盐酸的体积大于无气体产生消耗的盐酸的体积,说明该溶液中的溶质为K2SO3、KHSO3,盐酸先与K2SO3反应生成KHSO3,消耗盐酸25mL,再与亚硫酸氢根离子反应生成二氧化硫共消耗盐酸50mL,所以溶液中K2SO3、KHSO3的物质的量相等,最终得到溶液为氯化钾溶液,设K2SO3、KHSO3的物质的量均是x,则3x=0.075L×0.1mol/L,解得x=0.0025mol,所以产生二氧化硫的体积是2×0.0025mol×22.4L/mol=0.0112L=112mL;
②根据图像中的数据可知,生成气体消耗的盐酸的体积小于无气体产生消耗的盐酸的体积,说明溶液中的溶质为KOH、K2SO3;
③根据A曲线的结果可知K2SO3、KHSO3的物质的量均是0.0025mol,则K元素的物质的量是3×0.0025mol=0.0075mol,所以原KOH溶液的物质的量浓度为0.0075mol/0.05L=0.15mol/L。
考点:考查二氧化硫与氢氧化钾溶液反应的判断,产物的分析,对图像的分析判断及计算
本题难度:一般
3、选择题 下列各组物质中,所含分子数相同的是
A.10gH2和10g O2
B.5.6LN2(标况下)11gCO2
C.9gH2O和0.5gBr2
D.224mlH2(标况下)和0.1molN2
参考答案:B
本题解析:A、等质量,摩尔质量不等,故物质的量不等,分子数不等;
B、物质的量均为0.25mol,分子数相同;
C、H2O为0.5mol,溴为5g,分子数不等;
D、氢气为0.01mol,氮气0.1mol,不等
本题难度:一般
4、选择题 NA为阿伏加德罗常数,则下列说法错误的是(??)
A.1mol C2H5OH中一定含有NA个C2H5OH分子
B.将1mol HCl溶于一定量的水中,所得溶液中的H+的个数为NA
C.0.1 mol Na2O2中,阴离子的个数为0.1NA
D.1mol C在氧气中燃烧 ,转移的电子数一定为4 NA
,转移的电子数一定为4 NA
参考答案:D
本题解析:碳在氧气中燃烧有两种情况,当氧气不足量时得到的产物为CO,则转移的电子数为2NA,所以D项错误。乙醇属 于非电解
于非电解 质,
质,
本题难度:简单
5、选择题 用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.1 mol O3所含有的原子数为3NA
B.18克H2O中,原子数为2NA
C.22.4 L氯化氢所含的原子数为2NA
D.NA个 CH4分子的质量为16g/mol
参考答案:A
本题解析:
试题分析:臭氧含义3个氧原子,A不正确;18克H2O的物质的量是1mol,其中原子数为3NA,B不正确;C中氯化氢的条件不一定是在标准状况下,物质的量不一定是1mol,C不正确;D中质量的单位是g,D不正确,答案选A。
考点:考查阿伏加德罗常数的有关计算和判断
点评:阿伏加德罗常数是历年高考的“热点”问题,这是由于它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知识内容。要准确解答好这类题目,一是要掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系;二是要准确弄清分子、原子、原子核内质子中子及核外电子的构成关系。
本题难度:一般