A的质量分数
?
参考答案:BC
本题解析:
【错解分析】本题的误区多产生于由两种以上因素决定一个量的变化,由于分不清主、次,往往得出错误判断。如混合气体平均相对分子质量,它是由混合气体的总质量和混合气体的总物质的量两方面决定的。对于一般气相反应来说,只要产物不是液态或固态,混合气体的总质量就不变,而混合气体的总物质的量就视反应前后气体总体积数的变化,它决定了混合气体平均相对分子质量大小变化。如果有液、固相物质参与或生成,问题将变得更为复杂。又如浓度,若是单一种浓度引起平衡移动,其结果显而易见;若是加压引起,问题变为复杂。以教材的“针管实验”中二氧化氮为例,加压引起气体体积减小,气体的浓度增大;平衡移动,气体的浓度又减小,但该浓度比加压前大(本题B选项应为正确选项),比加压后平衡移动前的浓度小。反之减压的结果,气体的浓度由大变小(体积增大);由小变大(平衡移动),但移动后的浓度仍比减压前的小。再如物质的质量分数也是多因素决定的,它是由该物质的变化和所有物质的变化比较而得,因此判断容易产生失误。如加入C,增大C的浓度,平衡向逆反应方向移动。由于C增加的比平衡移动而引起A的增加要多,虽然A的浓度增大,物质的量增多,但A的质量分数并不增大。
【正解】本题是一道因外界条件改变,引起平衡移动的综合题。平衡移动必然引起浓度、质量分数、转化率……等量的变化,其中转化率……等是单因素引起变化(转化率中的变化量因条件而改变,而起始量不变),判断较为简单;而浓度、质量分数……等是诸多因素引起的变化(质量分数中的该物质和总物质都在变),必须找出其中主要因素,判断变化的结果。
本题难度:简单
2、选择题 对于反应:A2(g)+3B2(g) 2AB3(g);△H<0,如图所示,图中正确的是(????) 2AB3(g);△H<0,如图所示,图中正确的是(????)
参考答案:A
本题解析:该反应是放热反应,达平衡后,再升温,υ(正)、υ(逆)都增大,但υ(逆)增大的多,故A正确。增大压强,平衡向正反应方向移动,AB3%将增大,B2%将减小,故B、C不对。升温,平衡向逆反应方向移动,A2%、 B2%都增大,故C、D不对。
本题难度:一般
3、选择题 氨的催化氧化4NH3(g)+5O2(g)  4NO(g)+6H2O(g) ΔH=-1 025 kJ・mol-1是工业制备硝酸的重要反应。一定条件下将4 mol NH3和5 mol O2混合于固定容积为2 L的密闭容器中,经10 s该反应达平衡,并测得NO的浓度为0.8 mol・L-1。下列判断正确的是( )。 4NO(g)+6H2O(g) ΔH=-1 025 kJ・mol-1是工业制备硝酸的重要反应。一定条件下将4 mol NH3和5 mol O2混合于固定容积为2 L的密闭容器中,经10 s该反应达平衡,并测得NO的浓度为0.8 mol・L-1。下列判断正确的是( )。
A.以O2浓度变化表示的反应速率为0.064 mol・(L・s)-1
B.反应达到平衡状态时NH3的转化率为20%
C.升高温度能使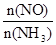 减小 减小
D.将容器的体积变为4 L,平衡时NO的浓度小于0.4 mol・L-1
参考答案:C
本题解析:
试题分析:??????????????? 4NH3(g)+5O2(g)  4NO(g)+6H2O(g) 4NO(g)+6H2O(g)
起始浓度(mol/L)????????? 2????? 2.5??????????? 0??????? 0
转化浓度(mol/L)???????? 0.8???? 1.0?????????? 0.8????? 0.8
平衡浓度(mol/L)???????? 1.2???? 1.5?????????? 0.8????? 0.8
则以O2浓度变化表示的反应速率为0.1 mol・(L・s)-1,A不正确;反应达到平衡状态时NH3的转化率为40%,B不正确;升高温度平衡向逆反应方向移动,则能使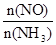 减小,C正确。将容器的体积变为4 L,平衡向正反应方向移动,平衡时NO的浓度大于0.4 mol・L-1,D不正确,答案选C。 减小,C正确。将容器的体积变为4 L,平衡向正反应方向移动,平衡时NO的浓度大于0.4 mol・L-1,D不正确,答案选C。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生解题方法与技巧的培养与训练,有利于培养学生的逻辑推理能力,提高学生的应试能力和学习效率。
本题难度:简单
4、选择题 在一固定容积的密闭容器中,放入3 L气体X和2 L气体Y,在一定条件下发生下列反应:4X(g)+3Y(g) 2Q(g)+nR(g)达平衡后,容器内温度不变,混合气体的压强比原来增大了5%,X的浓度减小 2Q(g)+nR(g)达平衡后,容器内温度不变,混合气体的压强比原来增大了5%,X的浓度减小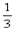 。则此反应中n值是(??? ) 。则此反应中n值是(??? )
A.3
B.4
C.5
D.6
参考答案:D
本题解析:略
本题难度:一般
5、选择题 一氧化氮与一氧化碳都是汽车尾气里的有害物质,它们能缓慢地起反应生成氮气和二氧化碳。对此反应,下列叙述中正确的是( )
A?使用催化剂能改变平衡常数?????? B?使用催化剂能改变反应速率
C?改变压强对反应速率没有影响???? D?降低压强能加大反应速率
参考答案:B
本题解析:平衡常数只与温度有关系,A不正确。有气体参加的反应,改变压强可以改变反应速率,C不正确。降低压强,反应速率降低,D不正确,所以正确的答案是B。
本题难度:一般
|