0.007
⑴NO的平衡转化率为_______
⑵下图中表示NO2的浓度变化曲线是????????????????????。
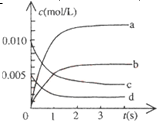
用O2表示从0~2s内该反应的平均速率v=????????????。
⑶能说明该反应已达到平衡状态的是?????????????????。
a.v (NO2)="2" v (O2)??????????? b.容器内压强保持不变
c.v逆?(NO)="2" v正 (O2)??????? d.容器内混合气体的密度保持不变
e.该容器内颜色保持不变
参考答案:(1)65%??(2分)??????(2)b????(2分)
本题解析:(1)根据表中数据可判断,平衡时NO的物质的量是0.007mol,所以消耗的NO是0.020mol-0.007mol=0.013mol,所以转化率是 。 。
(2)NO2是生成物,平衡时生成NO2是0.013mol,浓度是 ,所以曲线b表示NO2的浓度变化曲线。 ,所以曲线b表示NO2的浓度变化曲线。
(3)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。颜色的深浅和浓度大小有关系,所以选项e正确。A中速率的关系是恒成立的,不能说明。反应前后体积是变化的,所以压强也是变化的,因此当压强不再发生变化时,可以说明。C中反应速率的方向是相反的,且满足速率之比是相应的化学计量数之比,正确。混合气的密度是混合气的质量和容器容积的比值,在反应过程中,质量和容积都是不变的,所以密度始终是不变的,d不能正确。答案选bce。
本题难度:一般
2、选择题 在一体积固定容器内,对于N2(g)+3H2(g) 2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为( ) 2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为( )
A.断开1个N≡N键的同时有6个N―H键生成
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.N2、H2、NH3分子数之比1∶3∶2的状态
参考答案:C
本题解析:可逆反应达到化学平衡状态的实质是正逆反应速率相等但不为0。会生成断开1个N≡N键的同时,必然会生成2分子氨气,即6个N―H键生成,A不正确。密度是气体的质量和容器体积的比值,反应前后气体质量和容器体积均不变,所以在任何时刻混合气体的密度不变,B不正确。混合气体的平均相对分子质量是混合气的质量和混合气的物质的量的比值,质量不变,但物质的量是变化的,所以C可以说明。N2、H2、NH3分子数之比1∶3∶2的状态不一定满足正逆反应速率相等,D不正确。答案选C。
本题难度:简单
3、填空题 某一元弱酸(用HA表示)在水中的电离方程式是:HA H++A-,回答下列问题: H++A-,回答下列问题:
(1)向溶液中加入适量NaA固体, 以上平衡将向______(填“正”、“逆”)向移动,理由是______________________。
(2)若向溶液中加入适量NaCl溶液,以上平衡将向____(填“正”、“逆”)向移动,溶液中c(HA)将________(填“增大”、“减小”或“不变”),溶液中c(OH-)将______(填“增大”、“减小”或“不变”)。
(3)试设计实验方案证明HA为弱酸_______________________________________。
参考答案:(8分) (1)逆(1分) c(A-)增大,平衡向减小c(A
本题解析:
试题分析:(1) 加入NaA固体,A-增多,故平衡将向逆向移动,理由为c(A-)增大,平衡向减小c(A-)的方向移动即逆向移动。
(2)加入NaCl溶液,不反应,相当于加入水,溶液浓度变小,平衡将向正向移动,溶液中c(HA)将减小,c(H+)减小,则溶液中c(OH-)将增大。
(3) 证明HA为弱酸方法很多,比如:测0.1 mol・L-1 HA溶液的PH,若溶液的PH>1则它为弱酸。
点评:本题综合考查弱电解质的电离问题,题目较难,做题时注意把握“较强酸+较弱酸盐→较强酸盐+较弱酸”的反应规律。
本题难度:一般
4、选择题 在10℃时某化学反应速率为0.1mol/(L・min),若温度每升高10℃反应速率增加到原来的2倍。为了把该反应速率提高到1.6mol/(L・nim),则该反应需在什么温度下进行[???? ]
A.30℃
B.40℃
C.50℃
D.60℃
参考答案:C
本题解析:
本题难度:简单
5、选择题 下列平衡体系中,升温或减压都使平衡向正反应方向移动的是(△H<0表示放热):
A.N2(g)+3H2(g) 2NH3(g)△H<0 2NH3(g)△H<0
B.N2(g)+O2(g) 2NO3(g)△H<0 2NO3(g)△H<0
C.C(s)+H2O(g) CO2(g)+H2(g)△H>0 CO2(g)+H2(g)△H>0
D.2SO2(g)+O2(g) 2SO3(g)△H<0 2SO3(g)△H<0
参考答案:C
本题解析:略
本题难度:简单
|