微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (7分)德国克莱斯公司成功研制了利用甲醇车载制氢氧燃料电池工艺,其原理如右图所示,请观察此图回答:
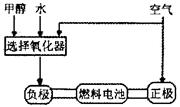
(1)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=" +" 49.0 kJ・mol-1
②2CH3OH(g)+O2(g)=2CO2(g)+4H2(g);△H=-385.8kJ・mol-1
下列说法正确的是
A.反应①中反应物的总能量高于生成物的总能量
B.反应①中拆开CH3OH(g)和H2O(g)中的化学键所需能量大于形成CO2(g)和3H2(g)中的化学键所释放的能量
C.CH3OH蒸气的燃烧热为大于192.9 kJ・mol-1
D.根据②推知反应:2CH3OH(l)+ O2(g)=2CO2(g)+4H2(g)的△H>-385.8kJ・mol-1
(2)最近科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。若有2.2kg CO2与足量H2恰好完全反应,生成气态的水和甲醇,可放出2473.5 kJ的热量,试写出合成塔中发生反应的热化学方程式???????????????。
(3)可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如右图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O。b处通入的物质是????,负极反应为:??????????????????????。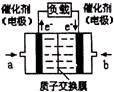
参考答案:(1) BC D (2分)
(2)CO2(g)+ 3H
本题解析:略
本题难度:简单
2、选择题 (10分)研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)利用反应6NO2+ 8NH3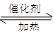 7N2+12 H2O可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
7N2+12 H2O可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
(2)已知:2SO2(g)+O2(g)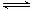 2SO3(g) ΔH=―196.6 kJ・mol-1
2SO3(g) ΔH=―196.6 kJ・mol-1
2NO(g)+O2(g)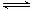 2NO2(g) ΔH=―113.0 kJ・mol-1
2NO2(g) ΔH=―113.0 kJ・mol-1
则反应NO2(g)+SO2(g)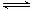 SO3(g)+NO(g)的ΔH= kJ・mol-1。
SO3(g)+NO(g)的ΔH= kJ・mol-1。
(3)铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O= Fe(OH)2+2Ni(OH)2
当电池放电时,正极电极反应式为 。
参考答案:(共10分)
(1)6.72(3分)
(2)-
本题解析:
⑴NO2在标准状况下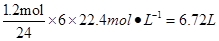
⑵①2SO2(g)+O2(g)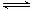 2SO3(g) ΔH=―196.6 kJ・mol-1
2SO3(g) ΔH=―196.6 kJ・mol-1
②2NO(g)+O2(g)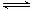 2NO2(g) ΔH=―113.0 kJ・mol-1
2NO2(g) ΔH=―113.0 kJ・mol-1
(①
本题难度:困难
3、填空题 (10分)碳、氮元素及其化合物与人类的生产生活密切相关。试回答下列有关问题:
(1)??????????NH3极易溶于水,其水溶液俗称氨水。用水稀释0.1mol・L―1的氨水,溶液中随着水量的增加而减小的是_____________(填序号)

(2)标准状况下,将1.12LCO2通入100mL1mol・L―1的NaOH溶液中,所得溶液中离子浓度由大到小的顺序为_________________________________________________;
①c(OH―)=2c(H2CO3)+______________________________________________;
②c(H+)+c(Na+)=___________________________________________________。
(3)甲烷燃料电池中发生的化学反应为:CH4+2O2=CO2+2H2O,该电池的电解质溶液为H2SO4溶液,则 原电池工作时电解质溶液中向正极移动的离子是_____________。
原电池工作时电解质溶液中向正极移动的离子是_____________。
参考答案:(1)b、d(2分,答对1个得1分,答错1个得0分)
本题解析:略
本题难度:简单
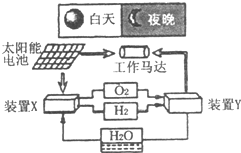
4、选择题 如图是一种航天器能量储存系统原理示意图.下列说法正确的是( )
A.装置X每消耗1mol?H2O,就可为燃料电池提供22.4?L燃料
B.该系统中最多存在3种形式的能量转化
C.装置Y中正极的电极反应式为:O2+2H2O+4e-→4OH-
D.装置X、Y形成的子系统实现了物质的零排放,并能实现化学能与电能间的完全转化
参考答案:A、装置X每消耗1molH2O,可生成1molH2,0.5m
本题解析:
本题难度:简单
5、填空题 (7分)
熔融碳酸盐燃料电池(MCFS),发明于1889年。现有一个碳酸盐燃料电池,以一 定比例Li2CO3和Na2CO3熔融混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为1:1)直接作燃料,其工作原理如图所示。
定比例Li2CO3和Na2CO3熔融混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为1:1)直接作燃料,其工作原理如图所示。

请回答下列问题:
(1)B极发生____(填“氧化”或“还原”)反应
(2)电池总反应为___________________________________________。
(3)以 此电源电
此电源电 解足量的CuSO4溶液,阳极产生气体0.56 L(已换算为标况),则阴极产物的质量为???????g。电解后溶
解足量的CuSO4溶液,阳极产生气体0.56 L(已换算为标况),则阴极产物的质量为???????g。电解后溶 液体积为1 L,溶液的pH约为???????。
液体积为1 L,溶液的pH约为???????。
(4)电池中的电解质碳酸钠形成的水溶液体系不能用带玻璃塞的试剂瓶保存,其原因是
????????????????????????????????????????(用化学方程式表示)
参考答案:
 本题解析:略
本题解析:略
本题难度:一般