微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 向恒温、恒容(2L)的密闭容器中充入2molX和一定量的Y,发生反应:2X(g)+Y(g)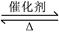 2Z(g)??ΔH<0,4mi n后达到平衡c(X)=0.2mol・L-1,且X与Y的转化率相等。下列说法中不正确的是
2Z(g)??ΔH<0,4mi n后达到平衡c(X)=0.2mol・L-1,且X与Y的转化率相等。下列说法中不正确的是
A.达到平衡时,再充入1molX,反应的焓变保持不变
B.用Y表示4min内的反应速率为0.1 mol・L-1・m in-1
C.再向容器中充 入1molZ,达到新平衡,c(X)∶c(Y)= 2∶1
D.4min后,若升高温度,平衡常数K增大
参考答案:D
本题解析:
试题分析:X与Y的转化率相等,说明Y加入的量为1mol,反应的焓加入的反应为的量无关,所以达到平衡时,再充入1molX,反应的焓变保持不变,故A正确;c(X)=0.2mol・L-1,
v(Y)=v(X)=×(2/2-0.2)/4=0.1 mol・L-1・m in-1,故B正确;再向容器中充 入1molZ,因为刚开始Y加入的量为1mol,所以达到新平衡,c(X)∶c(Y)= 2∶1,故C正确;2X(g)+Y(g)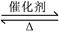 2Z(g)??ΔH<0,该反应为放热反应,所以升高温度,平衡常数K减小,故D错误,为本题的答案。
2Z(g)??ΔH<0,该反应为放热反应,所以升高温度,平衡常数K减小,故D错误,为本题的答案。
点评:本题考查了化学平衡,该考点是高考考查的重点和难点,本题有一定的综合性,该题难度适中。
本题难度:一般
2、选择题 把3mol P和2.5mol Q置于2L密闭容器中,发生如下反应:
3P(g)+Q(g) xM(g)+2N(g),5min后达到平衡生成1mol N,经测定这5min内 M的平均速率是0.1mol/(L・min),下列叙述错误的是(????)
xM(g)+2N(g),5min后达到平衡生成1mol N,经测定这5min内 M的平均速率是0.1mol/(L・min),下列叙述错误的是(????)
A.5min内P的平均反应速率为0.15mol/(L・min)
B.Q的转化率为25%
C.Q的平衡浓度为1mol/L
D.x是2
参考答案:B
本题解析:根据M的反应速率可知,生成M是0.1mol/(L・min)×2L×5min=1mol,根据变化量之比是相应的化学计量数之比可知,x=2。生成1molN的同时,消耗0.5molB,所以B的转化率是20%,B不正确。B的平衡浓度是2mol÷2L=1mol/L,C正确。反应速率之比是相应的化学计量数之比,因此A正确,答案选B。
本题难度:一般
3、计算题 二氧化氮在加热条件下能够分解成一氧化氮和氧气。该反应进行到45 s时,达到平衡(NO2浓度约为
0.0125 mol/L)。下图中的曲线表示二氧化氮分解在前25s内的反应进程。
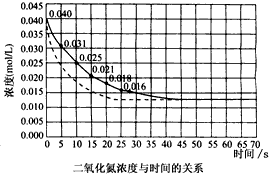
(1)请计算前20s内氧气的平均生成速率。
(2)若反应延续至70 s,请在图中用实线画出25s至70s的反应进程曲线。
(3)若在反应开始时加入催化剂(其他条件都不变),请在图上用虚线画出加入催化剂后的反应进程曲线。
(4)写出该反应的化学平衡常数表达式__________。
参考答案:(1)5.5×10-4mol/(L・s)
(2)下图中
本题解析:
本题难度:一般
4、填空题 已知下列两个反应:
反应Ⅰ:CO2(g)+H2(g)  CO(g)+H2O ΔH1
CO(g)+H2O ΔH1
反应Ⅱ:CO(g)+H2O(g)  CO2(g)+H2(g) ΔH2
CO2(g)+H2(g) ΔH2
(1)相同温度下,若上述反应Ⅰ的化学平衡常数为K1,反应Ⅱ的化学平衡常数为K2,那么K1・K2=________。
(2)反应Ⅰ化学平衡常数K1和温度t的关系如下表一:
t/℃
| 700
| 800
| 850
| 1 000
| 1 200
|
K1
| 0.6
| 0.9
| 1.0
| 1.7
| 2.6
?
该反应的ΔH1__________0(选填“>”、“=”或“<”)。
(3)某温度下,反应Ⅰ的化学平衡常数为2.25。在该温度下,向甲、乙、丙三个恒容密闭容器中通入CO2(g)和H2(g),这两种物质的起始浓度如下表二:
起始浓度
| 甲
| 乙
| 丙
| c(CO2)(mol/L)
| 0.01
| 0.02
| 0.02
| c(H2)(mol/L)
| 0.01
| 0.01
| 0.02
?
反应速率最快的是________(填“甲”、“乙”或“丙”),平衡时,H2转化率最大的是________(填“甲”、“乙”或“丙”),丙中H2的转化率为________。
参考答案:(1)1 (2)> (3)丙 乙 60%
本题解析:(1)反应Ⅰ和反应Ⅱ是一个反应,而且温度相同,只是表达方式有差别,反应Ⅰ的反应物是反应Ⅱ的生成物,故K1与K2互为倒数的关系。
(2)由表中温度与化学平衡常数的关系可知,温度越高,化学平衡常数(K)越大,即升高温度,平衡向正反应方向移动,故正反应为吸热反应,ΔH>0。
(3)丙中的CO2(g)和H2(g)起始浓度都最大,而反应温度相同,故丙中反应速率最大。甲、丙为等效平衡,而乙中CO2(g)的浓度大于H2(g)的浓度,故乙中H2转化率最大。
设丙中平衡时CO(g)的浓度为x mol/L,那么CO2(g)的浓度为(0.02 -x)mol/L,H2(g)的浓度为(0.02-x)mol/L,H2O(g)的浓度为x mol/L,
所以K=x2/(0.02-x)2=2.25,解得x=0.012,
即H2(g)的浓度为0.008 mol/L,
故丙中H2的转化率为×100%=60%。
本题难度:一般
5、选择题 某温度下,在甲、乙、丙三个恒容密闭容器中投入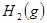 和 和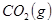 ,发生反应 ,发生反应 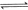 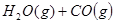 ,其起始浓度如下表所示。测得平衡时甲中 ,其起始浓度如下表所示。测得平衡时甲中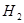 的转化率是60%。下列判断正确的是 的转化率是60%。下列判断正确的是
|
|
网站客服QQ: 960335752 - 14613519 - 791315772