微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 恒温条件下,将2.0molSO2与amolO2混合通入一密闭容器中,发生如下反应:2SO2(g)+O2(g) 2SO3(g)。反应达平衡时,测得容器内n(SO3)=1.3mol,n(O2)=3.0mol。
2SO3(g)。反应达平衡时,测得容器内n(SO3)=1.3mol,n(O2)=3.0mol。
求:⑴a的值。
⑵平衡时SO2的转化率。
参考答案:(1)3.65mol????(2)65%
本题解析:
试题分析:(1)???? 2SO2(g)+O2(g)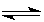 2SO3(g)
2SO3(g)
起始量(mol)??????2.0?????? a???????? 0
变化量(mol)??????1.3????? 0.65?????? 1.3
平衡量(mol)?????0.7?????? 3.0??????? 1.3
则a=3.0mol+0.65mol=3.65mol
(2)平衡时SO3的转化率=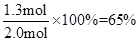
点评:在进行可逆反应的有关计算时,一般采用“三段式”进行,即分别列出起始量、转化量和平衡量或某深刻的量,然后依据已知条件列式计算即可。
本题难度:一般
2、计算题 (7分)某固定容积的2L密闭容器中进行反应 :?起始时加入的N2、H2、NH3均为2mol,5min后反应达到平衡, NH3的物质的量为3mol,求:
:?起始时加入的N2、H2、NH3均为2mol,5min后反应达到平衡, NH3的物质的量为3mol,求:
(1)这5分钟内用N2来表示该反应的反应速率(请写出计算过程,下同)
(2)求平衡时H2的物质的量浓度
(3)平衡时容器的压强为初始时的几分之几?
参考答案:(1)(2分)0.05mol/(L・min)??
(2
本题解析:略
本题难度:简单
3、选择题 对于反应A2 + 3B2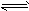 2C来说,以下化学反应速率的表示中,反应速率最快的是
2C来说,以下化学反应速率的表示中,反应速率最快的是
[???? ]
A.v(B2) =0.8mol/(L・s)
B.v(A2) =0.4mol/(L・s)
C.v(C) =0.6mol/(L・s)
D.v(B2) =4.2mol/(L・min)
参考答案:B
本题解析:
本题难度:简单
4、填空题 (每空2分,共18分)在实验室中做如下实验:一定条件下,在容积为2.0L的恒容密闭容器中,发生如下反应: 2A(g)+ B(g)2C(g);?△H=QkJ/mol
B(g)2C(g);?△H=QkJ/mol
(1)若A、B起始物质的量均为零,通入C的物质的量(mol)随反应时间(min)的变化情况如下表:
 实验 实验
序号
| ?
| 0
| 10
| 20
| 30
| 40
| 50
| 60
|
1
| 8 0 0 ℃
| 1.0
| 0.80
| 0.67
| 0.57
| 0.50
| 0.50
| 0.50
|
2
| 8 0 0 ℃
| n2
| 0.60
| 0.50
| 0.50
| 0.50
| 0.50
| 0.50
|
3
| 8 0 0 ℃
| n3
| 0.92
| 0.75
| 0.63
| 0.60
| 0.60
| 0.60
|
4
| 7 3 0 ℃
| 1.0
| 0.90
| 0.80
| 0.75
| 0.70
| 0.65
| 0.65
|
根据上表数据,完成下列填空:
①在实验1中反应在10至20min内反应的平均速率Vc=????mol/(L・min);实验2中采取的措施是??????????;实验3中n3?????1.0 mol(填“>、=、<”)。
②比较实验4和实验1,可推测该反应中Q_??0(填“>、=、<”),理由是_?
????????????????????????????????????
(2)在另一反应过程中A(g)、B(g)、C(g)物质的量变化如右图所示,根据图中所示判断下列说法正确的__?__。
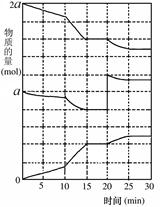
a.10~15 min可能是升高了温度??
b.10~15 min可能是加入了催化剂
c.20 min时可能是缩小了容器体积????
d.20 min时可能是增加了B的量
(3)一定条件下,向上述容器中通入5molA (g)和3molB(g),此时容器的压强为P(始
(g)和3molB(g),此时容器的压强为P(始 )。
)。
反应进行并达到平衡后,测得容器内气体压强为P(始)的 。若相同条件下,向上述
容器中分别通入a molA(g)、b molB(g)、c molC(g),欲使达到新平衡时容器内气体压
强仍为P(始)的 。
①a、b、c必须满足的关系是?????????????,????????????????。
(一个用a、 c表示,另一个用b、c表示)
c表示,另一个用b、c表示)
②欲使起始时反应表现为向正反应方向进行,则a的取值范围是????????????。
参考答案: 本题解析:略
本题解析:略
本题难度:一般
5、填空题 将2 mol H2O和2 mol CO置于1 L容器中,在一定条件下,加热至高温,发生如下可逆反应:
2H2O(g) 2H2+O2???????????2CO+O2
2H2+O2???????????2CO+O2 2CO2
2CO2
(1)当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是___________和___________,或___________和___________。(填它们的分子式)
(2)若平衡时O2和CO2的物质的量分别为n(O2)平=a mol,n(CO2)平=b mol。试求n(H2O)平="______" 。(用含a、b的代数式表示)
参考答案:(1)H2和H2O,或CO和CO2
(2)2-2
本题解析:(1)在同一反应容器连续发生了两个反应。只有H2O(g)分解了,CO才能被O2氧化。两反应相互制约,同时达到平衡。但第一反应中H2O和H2与第二个反应无关,同样第二个反应中CO和CO2的浓度与第一个反应无关。(2)从原子守恒角度分析,由CO生成CO2分子内增加的氧原子来源H2O,另外O2中的氧也来源于H2O。因此,n(H2O)反应=2n(O2)+n(CO2)=(2a+b) mol。所以n(H2O)平=[2-(2a+b)] mol。
本题难度:一般