��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� 23.75gij�����۽������Ȼ��MCl2���к���3.01��1023��Cl-����MCl2��MԪ��Ϊ
A��Cu
B��Mg
C��Fe
D��Zn
�ο��𰸣�B
���������3.01��1023��Cl-�����ʵ���Ϊ0.5mol����MCl2�����ʵ���Ϊ0.25mol�����ɵ�MCl2����Է�������Ϊ��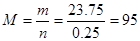 ������MԪ��ԭ�ӵ����ԭ������Ϊ24������MԪ��ΪþԪ�أ�
������MԪ��ԭ�ӵ����ԭ������Ϊ24������MԪ��ΪþԪ�أ�
�����Ѷȣ�һ��
2��ѡ���� ��5ml���ʵ���Ũ��Ϊ18.4mol/L��Ũ�������ˮ�У�ϡ�ͳ�100ml��Һ������ϡ��������ʵ���Ũ���ǣ�������
A��0.46mol/L
B��0.92mol/L
C��4.6mol/L
D��5mol/L
�ο��𰸣���ϡ�ͺ�������Һ��������Ũ��Ϊc����
5mL��18.
���������
�����Ѷȣ���
3��ѡ���� ����˵����ȷ����(??? )
A�����ʵ�������һ����������ʵ�����
B�������ӵ���������6.02��1023
C���Ƶ�Ħ�����������������ԭ������
D���ڱ�״���£�1 mol�κ�����������ԼΪ22.4 L
�ο��𰸣�D
���������A������ȷ�� ���ʵ����DZ�ʾ������������(N)���磺���ӣ�ԭ�ӵȣ��밢���ӵ�����(NA)֮�ȣ���n=N/NA�� B������ȷ�������ӵ���������6.02��1023mol�D1; C������ȷ�� �����ʵ������Կ�Ϊ��λʱ��Ħ�������ĵ�λΪg/mol������ֵ�ϵ��ڸ����ʵ����ԭ����������Է���������D����ȷ��
�����Ѷȣ�һ��
4�������� ��һ����汻�����������ƵĽ����ƣ�������10.8g������Ͷ�뵽100gˮ����ȫ��Ӧ���ռ���0.2g�������õ��ܶ�Ϊ1.106g��cm3����Һ���Լ���(Ҫ��д����)��?
��1��10.8g�����У������Ƶ������Ƕ��ٿ�?
��2����Ӧ��������Һ�����ʵ����ʵ���Ũ��Ϊ���٣�
�ο��𰸣���1��4��6g??��2��4mol��L
���������
�����������1��������Ƶ�����Ϊm�����ݷ�Ӧ�Ļ�ѧ����ʽ���㣬
2Na+2H2O�T2NaOH+H2��
2��23g??????????? 2g
m?????????????? 0.2g
m=4.6g
��δ�����Ľ�����Ϊ4.6g��
��2��n��Na��=0.2mol��������m��Na20��=10.8g-4.6g=6.2g? n��Na20��=0.1mol�ɷ�Ӧ2Na+2H2O�T2NaOH+H2����Na2O+H2O�T2NaOH��֪��Һ�����ʵ����ʵ���Ϊ��n��NaOH��=0.
�����Ѷȣ�һ��
5��ѡ���� ���1gˮ�к���n����ԭ�ӣ����ӵ������� �� ��
A��n/1mol��1 B��9n mol��1 C��2nmol��1 D��nmol��1
�ο��𰸣�B
�����������
�����Ѷȣ�һ��