微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (7分)某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。
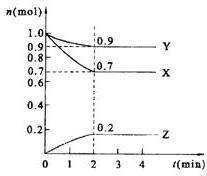
①由图中所给数据进行分析,该反应的化学方程式为??????????????????????????????????;
②?反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=???????????????,
③当反应进行了3 min,该反应是否达到平衡??????????(填“是”或“否”)。
(2)把除去氧化膜的镁条投入到盛有稀盐酸的试管中,发现H2生成的速率变化情况如图,其中
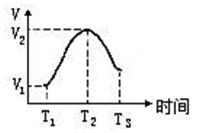
T1~T2速率变化的主要原因是__???????????????????????????__,?
T2~T3速率变化的主要原因是___?? ___??????????????????????????
参考答案:(1)①3X+Y  本题解析:略
本题解析:略
本题难度:一般
2、选择题 一定温度下,在恒容密闭容器中发生如下反应:2X(g)+Y(g) 3Z(g),若反应开始时充入2mol X和2mol Y,达平衡后Y的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后Y的体积分数>a%的是
3Z(g),若反应开始时充入2mol X和2mol Y,达平衡后Y的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后Y的体积分数>a%的是
A.1molY,1molZ
B.2mol X,1molY,1molZ
C.1molY和3molZ
D.2molZ
参考答案:A
本题解析:考查等效平衡的判断。根据方程式可知,反应前后体积不变的,所以要满足平衡等效,则换算后的物质的量之比和原平衡相同即可。据此可知ABCD分别相当于2/3molX和4/3molY、8/3molX和4/3molY、2molX和2molY、4/3molX和2/3molY,所以A正确,BD均是<a%,C是=a%,答案选A。
本题难度:一般
3、选择题 可逆反应①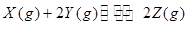 、②
、②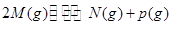 分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
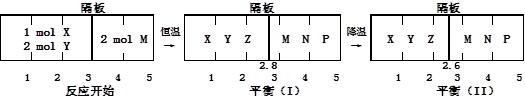
下列判断正确的是:
A.反应①的正反应是吸热反应
B.在平衡(I)和平衡(II)中的气体摩尔体积相同
C.达平衡(I)时X的体积分数为5/11
D.达平衡(I)时体系的压强与反应开始时体系的压强之比为10:11
参考答案:D
本题解析:
试题分析:反应过程中①气体物质的量减少,②气体物质的量不变。A、平衡(I)降温至平衡(II),左室气体物质的量减少,平衡正向进行,反应放热,错误;B、平衡(I)和平衡(II)右室物质的量相同,体积不同,故气体摩尔体积不同,错误;
C、根据阿伏伽德罗定律,同温同压下气体体积比等于物质的量比,得出反应后左室物质的量为28/11mol,??? X+2Y?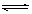 2Z?
2Z?
始量???1????? 2
转化量? a????? 2a??????? 2a
平衡量 1-a???? 2-2a?????? 2a
1-a+2-2a+2a=28/11??? a=5/11
平衡(I)时X的体积分数为6/11÷28/11=3/14,错误;
D、同温同压下气体压强比等于物质的量比,达平衡(I)时体系的压强与反应开始时体系的压强之比为(3+2):(2+28/11)=10:11,正确。
本题难度:一般
4、选择题 在恒温下的密闭容器中,有可逆反应2NO(g)+O2(g) 2NO2(g),不能说明该反应已达到平衡状态的是(?????? ) ??????????????????????????????????????????????
2NO2(g),不能说明该反应已达到平衡状态的是(?????? ) ??????????????????????????????????????????????
A.混合气体的颜色不再变化
B.反应器中的压强不随时间的变化而变化
C.混合气体中NO2的体积分数保持不变
D.生成NO2的速率与生成O2的速率相等
参考答案:D
本题解析:颜色不再变化,即说明浓度不再变化,A可以。反应前后体积是变化的,即压强是变化的,当压强不再变化时,可以说明。物质当体积分数不再变化,即说明反应已经达到平衡状态。选项D中当反应速率方向相反,但不满足速率之比是相应但化学计量数之比,即正逆反应速率不相等,所以不能说明。答案选D。
本题难度:一般
5、选择题 在温度压强不变的情况下,已知N2O4 ??????2NO2,2mol N2O4在密闭容器内分解成NO2,到达平衡时生成了0.6mol NO2,则平衡时气体的总物质的量是(???)
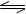
A.0.6mol
B.1.8mol
C.2.2mol
D.2.3mol
参考答案:D
本题解析:
试题分析:平衡时生成了0.6mol二氧化氮气体,所以反应的四氧化二氮为0.3mol,剩余的四氧化二氮气体为1.7mol,气体总物质的量为(0.6+1.7)mol。
点评:平衡时体系中有二氧化氮和四氧化二氮两种气体。
本题难度:一般