微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水中的沉淀溶解平衡曲线见下图。下列说法正确的是 ( )
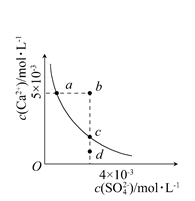
A.在任何溶液中,c(Ca2+)、c(SO42―)均相等
B.b点将有沉淀生成,平衡后溶液中c(SO42―)一定等于3×10-3mol・L-1
C.a点对应的Ksp等于c点对应的Ksp
D.d点溶液通过蒸发可以变到c点
参考答案:C
本题解析:A项只有在CaSO4溶液中c(Ca2+)、c(SO42―)才相等;B项b点Qc>Ksp,故有沉淀生成,开始时,c(Ca2+)、c(SO42―)不相等,而反应消耗的Ca2+、SO42―相等,因此平衡后的两种离子的浓度不会都等于3×10-3mol・L-1,B项错误;在平衡线上的点对应的Ksp均相等,C项正确;D项d点溶液通过蒸发后各离子浓度都增大,不可能保持SO42―浓度不变而到达c点,D项错误。
本题难度:一般
2、选择题 常温下,Ksp(CaSO4)=9?10-6,常温下CaSO4在水中的沉淀溶解平衡曲线见图。下列说法正确的是
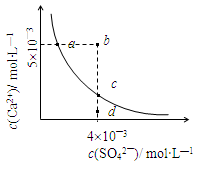
A.常温下CaSO4饱和溶液中,c(Ca2+)、c(SO42―)对应于曲线上任意一点
B.b点将有沉淀生成,平衡后溶液中c(SO42―)等于3?10-3 mol・L―1
C.d点溶液通过蒸发可以变到c点
D.a点对应的Ksp等于c点对应的Ksp
参考答案:D
本题解析:A.常温下CaSO4饱和溶液中,对应c(Ca2+)=c(SO42―)=3?10-3 mol・L―1的这一点,不正确
B:B点溶液中离子积大于9×10-6,所以一定有沉淀析出。由于起始时c(SO42-)小于c(Ca2+),所以平衡时c(SO42-)仍然小于c(Ca2+),即c(SO42-)小于3×10-3 mol/L,B不正确
C:蒸发过程中c(SO42-)应该是增大的,所以选项C不正确。
D:溶度积常数只与温度有关系,所以选项D正确
答案为D
本题难度:一般
3、选择题 常温下,对于醋酸溶液的下列说法中,不正确的是
A.0.1 mol・L-1的醋酸溶液中加水稀释,溶液中c(OH-)减小
B.醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-)
C.pH=4的醋酸溶液与pH=10的烧碱溶液等体积混合后溶液呈酸性
D.醋酸溶液中加入少量醋酸钾晶体,醋酸电离程度减小
参考答案:A
本题解析:醋酸是弱酸,存在电离平衡,稀释促进电离,但氢离子的浓度降低,所以c(OH-)增大,A不正确。C符合电荷守恒,正确。pH=4的醋酸溶液的浓度大于0.0001mol/L,所以反应中醋酸是过量的,溶液显酸性,C正确。增大醋酸根离子的浓度抑制醋酸的电离,D正确,答案选A。
本题难度:简单
4、选择题 已知BaCO3和BaSO4均为难溶电解质,其溶度积分别为Ksp(BaCO3)=5.1×10-9 mol2・L-2,Ksp(BaSO4)=1.1×10-10 mol2・L-2,则下列说法中正确的是(??)
A.BaSO4可做钡餐而BaCO3不能是因为Ksp(BaSO4)<Ksp(BaCO3)
B.在制腈纶纤维的1 L溶液中含SO42-为1.0×10-3 mol,则加入0.01 mol BaCl2不能使SO42-完全沉淀
C.在清理有关仪器的BaSO4沉淀时,常加入饱和Na2CO3溶液,使BaSO4转化为BaCO3再用酸处理
D.用稀H2SO4洗涤BaSO4效果比用水好,BaCO3也能用此法处理
参考答案:C
本题解析:A、是因为BaSO4比BaCO3稳定;
B、加入0.01molBaCl2,c(SO)===1.1×10-7,符合要求。
C、饱和Na2CO3溶液,增加碳酸根浓度,可以将BaSO4转化为BaCO3。
D、BaCO3溶于酸,故不能使用该方法。
本题难度:一般
5、选择题 石灰乳中存在下列平衡:Ca(OH)2(s)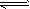 Ca2+(aq) +2OH-(aq),加入少量下列固体物质,可使Ca(OH)2减少的是 [???? ]
Ca2+(aq) +2OH-(aq),加入少量下列固体物质,可使Ca(OH)2减少的是 [???? ]
A. Na2CO3
B. NaCl
C. NaOH
D. CaCl2
参考答案:A
本题解析:
本题难度:一般