微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (12分)(1)H+可与H2O形成H3O+,H3O+中O原子采用???? ??????杂化,其键角比水分子?????(填“大”或“小”)。
??????杂化,其键角比水分子?????(填“大”或“小”)。
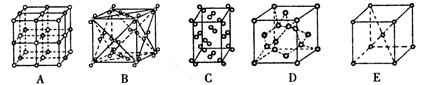
(2)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞示意图(未按顺序排序)。上述五种晶体中晶体类型相同的是????????????????????;(填写编号)。
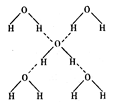
(3)在冰的晶体中,每个水分子与相邻的 4 个水分子形成氢键(如图所示),已知冰的升华热(即 1 mol 水由冰转化为水蒸汽所需能量)是51KJ/mol,除氢键外,水分子间还存在范德华力(11 kJ / mol ) , 则冰晶体中氢键的“键能”(破坏 lmol 氢键所需的能量即为 氢键的“键能”)是????????????????kJ / mol 。
氢键的“键能”)是????????????????kJ / mol 。
(4)CaO与NaCl的晶胞同为面心立方结构,已知CaO晶体密度为ag・cm-3,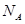 表示阿伏加德罗常数,则CaO晶胞体积为???????cm3。
表示阿伏加德罗常数,则CaO晶胞体积为???????cm3。
(5)在酸性溶液中,发生的氧化还原反应中被氧化与被还原的的元素的物质的量之比为2:5,
□KBiO3+□MnSO4+□H2SO4==□Bi2(SO4)3+□????+□????+□????????????????????????????????
写出Bi同主族第四周期元素的电子排布式:???????????????????????????
参考答案:(12分)(1) 本题解析:略
本题解析:略
本题难度:简单
2、选择题 下列物质中不含共价键的是[???? ]
A.NH4Cl
B.NaOH
C.KBr
D.Na2O2
参考答案:C
本题解析:
本题难度:简单
3、选择题 碲(Te)是第52号元素,位于周期表中第VIA族,处于金属区与非金属区的交界线上.下列叙述正确的是( )
A.碲的单质具有半导体的性能
B.碲化氢(H2Te)比H2S更稳定
C.碲可在空气中燃烧生成二氧化碲(TeO2)
D.H2TeO4的酸性比H2SO4强
参考答案:AC
本题解析:
本题难度:简单
4、选择题 下面的叙述正确的是? [???? ]
A.两种非金属元素原子之间形成的化学键不一定都是极性键
B.共价化合物中可能含有离子键
C.只要是离子化合物其熔点就比共价化合物的熔点高
D.将某种化合物溶于水,若能导电说明这种化合物是离子化合物
参考答案:A
本题解析:
本题难度:简单
5、选择题 下列化学用语正确的是 [???? ]
A.乙烯的结构简式为:CH2CH2
B.苯酚的分子式为:C6H6O
C.羟基的电子式为:-O:H
D.甲烷分子的比例模型:
参考答案:B
本题解析:
本题难度:简单