微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 某配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1。其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)dn+6nsl,回答下列问题。
(1)元素B、C、D的第一电离能的由大到小排列顺序为??????。(用元素符号表示)
(2)D元素原子的最外层电子排布图为?????????????????????????。
(3)该配位化合物的化学式为??????,配体的中心原子的杂化方式为?????。
(4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1:1和l:2,两种化合物可任意比互溶,解释其主要原因为?????????????????????????????。
(5)A元素与B元素可形成分子式为A2B2的某化合物,该化合物的分子具有平面结构,则其结构式为?????????,分子中含有???????个s键,???????个p键。
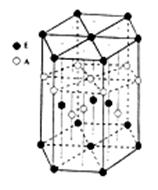
(6)A元素与E元素可形成一种红色化合物,其晶体结构单元如图。则该化合物的 化学式为????????。该化合物可在氯气中燃烧,生成一种棕黄色固体和一种气体,写出该反应的化学方程式???????????。
参考答案:(1)N>O>S (2分)??(2)![]()
本题解析:
试题分析:原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1。其中C、D元素同主族且原子序数D为C的二倍,判断D是S、C是O;E元素的外围电子排布为(n-1)dn+6nsl,n-1≥3,0<n+6≤10,n=4,故E是Cu。A在比例中相对很多,可能是H元素;将H、O、S、Cu(蓝色)的化合价+1、-2、+6、+2带入比例组成的H14B4O5SCu中,B为-3价,在O元素之前,是N元素。
本题难度:一般
2、填空题 Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
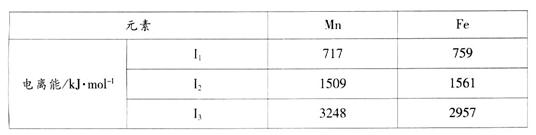
回答下列问题:
(1)Mn元素价电子的电子排布式为???????????????????????,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fen再失去一个电子难。其原因是???????????????。
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是????????????。
②络离子[Fe(CN)6]4-的配体CN-中C原子的杂化轨道类型是???????????,写出一种与 CN-互为等电子体的单质分子的电子式??????????????????????????。
(3)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁的晶体类型为????????????????。
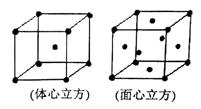
(4)金属铁晶体在不同的温度下有两种堆积方式,如图所示。体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为?????????????。
参考答案:(1)3d54s2(1分) 由Mn2+转化为Mn3+时,3d
本题解析:
试题分析:(1)Mn元素为2号元素,价电子的排布式为:3d54s2;Mn2+的价电子为3d5,3d轨道半充满,较稳定,由较稳定的3d5半充满态转为不稳定的3d4状态需要的能量较多;Fe2+的价电子为3d6,不稳定,由不稳定的3d6到稳定的3d5半充满状态,需要的能量相对要少。
(2)①Fe原子或离子外围有较多能量相近的空轨道,所以与Fe原子或离子形成配合物的分子或离子应具备的结构特征是具有孤对电子。
②CN-中C与N形成碳氮三键,所以C原子杂化方式为sp;原子数相等、价电子数相等的微粒
本题难度:一般
3、简答题 A、B、C、D分别代表四种不同的短周期元素.A元素的原子最外层电子排布为ns1,B元素的原子价电子排布为ns2np2,C元素的最外层电子数是其电子层数的3倍,D元素原子的M电子层的P亚层中有3个电子.
(1)C原子的电子排布式为______,若A元素的原子最外层电子排布为1s1,则按原子轨道的重迭方式,A与C形成的化合物中的共价键属于______键.
(2)当n=2时,B的原子结构示意图为______,B与C形成的晶体属于______晶体.当n=3时,B与C形成的晶体中微粒间的作用力是______
(3)若A元素的原子最外层电子排布为2s1,B元素的原子价电子排布为3s23p2,元素A在周期表中的位置是______,A、B、C、D四种元素的第一电离能由大到小的顺序是______(用元素符号表示).
参考答案:A、B、C、D分别代表四种不同的短周期元素.A元素的原子最外
本题解析:
本题难度:一般
4、选择题 下列说法错误的是( )
A.铅笔不含铅
B.水银不含银
C.白金不是金
D.火碱不是碱
参考答案:D
本题解析:
本题难度:简单
5、选择题 下列叙述正确的是 [???? ]
①两种原子构成的共价化合物分子中的化学键都是极性键
②两种不同非金属元素原子间形成的化学键都是极性键
③含有非极性键的化合物一定是共价化合物
④只要是离子化合物,其熔点就比共价化合物的熔点高
⑤难失?去电子的原子,易形成阴离子
⑥单质分子中不存在化学键,化合物的分子中才存在化学键
⑦离子化合物中一定含有离子键
A.只有②⑦??
B.只有①⑦
C.只有⑦??
D.只有①⑤⑦
参考答案:A
本题解析:
本题难度:简单