微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (共13分).Ⅰ(6分)、在淀粉KI溶液中加入少量NaClO溶液,并加入少量硫酸,溶液立即变蓝,所发生的离子方程式是?????????????????????????????????????,
在上述蓝色溶液中滴加足量的Na2SO3溶液,现象 是??????????? _______________________?,
是??????????? _______________________?,
所发生的离子方程式是????????????????????????????????????????。
Ⅱ(7分)、下面是你熟悉的物质:
① O2?②金刚石 ③ NaBr?④H2SO4?⑤ Na2CO3?⑥ Na2S?⑦ NaHSO4
这些物质中,只含共价键的是_______________;只含离子键的是_______________;既含共价键又含离子键的是________________(以上填序号)
参考答案:
Ⅰ、ClO-+2I-+2H+==Cl-+I2+H2O
本题解析:略
本题难度:一般
2、选择题 氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是
A.2Na2O2+2H2O =4NaOH+O2↑
B.Cl2 + H2O  HClO + HCl
HClO + HCl
C.2F2+2H2O=4HF+O2
D.4Fe(OH)2+O2+2H2O=4Fe(OH)3
参考答案:C
本题解析:
试题分析:目标方程式中水的作用是既非氧化剂又非还原剂,A、水的作用是既非氧化剂又非还原剂,错误;B、水的作用是既非氧化剂又非还原剂,错误;C、水在该反应中作还原剂,与目标方程式中水的作用不同,正确;D、水的作用是既非氧化剂又非还原剂,错误,答案选C。
本题难度:一般
3、填空题 现有溶质质量分数为98%、密度为1.84kg・L-1的浓硫酸,若用其配制1.0mol・L-1的稀硫酸250ml。回答下列问题:
(1)需要98%的浓硫酸???????ml(计算保留两位小数)。
(2)配制时,要用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需????????????。
参考答案:(1)13.6
(2)250 ml容量瓶,胶头滴管
本题解析:
试题分析:溶液在稀释前后溶质的物质的量不变。(1.84×103g/L×V×98%)÷98g/mol=0.25L×1.0mol/L.解得V="0.0136L=13.6ml." (2)在配制物质的量浓度的溶液时,要用到的玻璃仪器除量筒、烧杯、玻璃棒、胶头滴管、250 ml容量瓶。
本题难度:简单
4、选择题 下列有关表述正确的是(???)
A.次氯酸的电子式: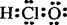
B.N原子的电子排布图为:
C.硫原子的价电子排布式:3s23p4
D.二氧化硅的分子式:SiO2
参考答案:C
本题解析:次氯酸的电子式H:O:Cl: ,A错;N原子的电子排布图为1s2 2s2 2p3 ,根据洪特规则2p应为半满,B错;硫原子的价电子排布式为3s23p4,C正确;二氧化硅是原子晶体,不存在单个分子结构(分子存在于分子晶体),SiO2仅仅体现了原子的个数比,是一个宏观的表示方法,并不是分子式,D错。故本题选C。
本题难度:简单
5、选择题 代硫酸钠可用作脱氯剂,已知25.0 mL 0.1 mol・L-1的Na2S2O3溶液恰好把标准状况下112 mL Cl2完全转化为Cl-时,S2O32-转化成( )
A.S2-
B.S
C.SO32-
D.SO42-
参考答案:C
本题解析:
试题分析:在氧化还原反应中氧化剂得到的电子与还原剂失去的电子的物质的量相等。假设反应后S元素的化合价为+X价。0.1mol/L×0.025L×2×(X-2)=0.112L÷22.4mol/L×2×1.解得+X=+4.分析选项中各物质中S元素的化合价可知SO32-正确。选项为C。
考点:考查氧化还原反应的电子守恒的知识。
本题难度:一般