微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列对四种溶液中的离子能否大量共存的评价正确的是
A.A
B.B
C.C
D.D
参考答案:D
本题解析:分析:根据离子之间不能结合生成水、气体、沉淀,不能发生氧化还原反应等,则离子能大量共存,以此来解答.
解答:A.因HCO3-、OH-结合生成水和碳酸根离子,则离子不能共存,故A错误;
B.滴入酚酞试液显红色的溶液中,显碱性,该组离子不反应,能共存,评价错误,故B错误;
C. =109的溶液,显碱性,Ca2+不能大量存在,评价错误,故C错误;
=109的溶液,显碱性,Ca2+不能大量存在,评价错误,故C错误;
D.pH=1的溶液中,H+、ClO-、Cl-发生氧化还原反应,不能共存,评价正确,故D正确;
故选D.
点评:本题考查离子的共存,明确习题中的信息及离子之间的反应是解答本题的关键,选项C为解答的难点和易错点,题目难度不大.
本题难度:困难
2、选择题  节能减排、低碳生活已经成为时尚.下列举措不符合这一要求的是
节能减排、低碳生活已经成为时尚.下列举措不符合这一要求的是
A.家庭出行、购物尽量使用可反复使用的布袋
B.为了能随时喝到热水,饮水机应24小时开启
C.日常生活中尽量使用二次电池,抵制使用一次电池
D.多用永久性的筷子、饭盒,尽量避免使用一次性的餐具
参考答案:B
本题解析:分析:节能减排重在节约能源,减少污染物的排放;
“低碳生活”指的是生活作息时所耗用的能量要尽量减少,特别是减少二氧化碳的排放量,减缓生态恶化;可以从节电、节能和回收等环节来改变生活细节;
解答:A、家庭出行、购物尽量使用可反复使用的布袋,可以减少“白色污染”,符合题意,故A正确;
B、为了能随时喝到热水,饮水机应24小时开启,浪费了节约能源,不符合题意,故B错误;
C、日常生活中尽量使用二次电池,抵制使用一次电池,节约能源,减少污染物的排放,符合题意,故C正确;
D、多用永久性的筷子、饭盒,尽量避免使用一次性的餐具,节约能源,减少污染物的排放,故D正确.
故选:B;
点评:本题是一道环保知识题目,可以根据所学知识来回答,注意知识的积累,难度不大.
本题难度:简单
3、选择题 由5mol?Fe2O3、4mol?Fe3O4和3mol?FeO组成的混合物,加入纯铁1mol并在高温下和Fe2O3反应.若纯铁完全反应,则反应后混合物中FeO与Fe2O3的物质的量之比可能是
A.4:3
B.3:2
C.3:1
D.2:l
参考答案:BC
本题解析:分析:根据在高温下可能发生Fe2O3+Fe 3FeO或4Fe2O3+Fe
3FeO或4Fe2O3+Fe 3Fe3O4时两种反应,或两种反应同时进行,根据加入铁的物质的量为1mol,结合化学方程式计算可能存在的物质的量的比值.
3Fe3O4时两种反应,或两种反应同时进行,根据加入铁的物质的量为1mol,结合化学方程式计算可能存在的物质的量的比值.
解答:分析题给混合物和高温下发生的反应,可知:
当发生反应:Fe2O3+Fe 3FeO时,反应后混合物中含有6molFeO、4molFe2O3,则FeO与Fe2O3的物质的量之比为3:2;
3FeO时,反应后混合物中含有6molFeO、4molFe2O3,则FeO与Fe2O3的物质的量之比为3:2;
当发生反应:4Fe2O3+Fe 3Fe3O4时,反应后混合物中含有3molFeO、1molFe2O3,则FeO与Fe2O3的物质的量之比为3:1;
3Fe3O4时,反应后混合物中含有3molFeO、1molFe2O3,则FeO与Fe2O3的物质的量之比为3:1;
当两反应均存在时,FeO与Fe2O3的物质的量之比处于两者之间,
故选BC.
点评:此题考查了化学计算知识,极端假设法是指根据已知的条件,把复杂问题假设为处于理想的极端状态,站在极端的角度去分析、考虑问题,使其因果关系显得十分明显、简单,从而迅速地作出正确判断的方法.比如此题中我们就假设了两个极端,首先确定两个极端,然后确定范围,最后选择.
本题难度:简单
4、选择题 将Na2CO3?10H2O与NaHCO3的混合物m?g溶解于水,配制成100mL溶液,测知溶液中Na+的质量m(Na+)=0.92g,若将溶液蒸干并加热至质量不变,可得固体的质量是
A.1.86g
B.2.55g
C.2.12g
D.无法确定
参考答案:C
本题解析:分析:将Na2CO3?10H2O与NaHCO3的混合物mg溶解于水,将溶液蒸干并加热至质量不变,最后得到的固体为Na2CO3,根据Na元素守恒可计算Na2CO3的物质的量,进而计算Na2CO3的质量.
解答:将Na2CO3?10H2O与NaHCO3的混合物mg溶解于水,将溶液蒸干并加热至质量不变,
NaHCO3加热分解生成Na2CO3,最后得到的固体为Na2CO3,
配制成100mL溶液,测知溶液中Na+的质量m(Na+)=0.92g,
则n(Na+)=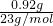 =0.04mol,
=0.04mol,
n(Na2CO3)= n(Na+)=0.04mol×
n(Na+)=0.04mol× =0.02mol,
=0.02mol,
m(Na2CO3)=0.02mol×106g/mol=2.12g,
故选C.
点评:本题考查混合物的计算,题目难度不大,本题注意加热后固体的成分的判断,根据Na元素守恒计算.
本题难度:一般
5、选择题 常温下,下列各组离子在指定溶液中能大量共存的是
A.c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO、Cl-
B.pH=1的溶液中:Fe2+、NO、SO、Na+
C.c(Fe3+)=0.1mol?L-1的溶液中:K+、ClO-、SO42-、SCN-
D.由水电离的c(H+)=1×10-14mol?L-1的溶液中:Ca2+、K+、Cl-、HCO
参考答案:A
本题解析:分析:A.c(H+)/c(OH-)=1012的溶液中,c(H+)=0.1mol/L,溶液显酸性;
B.pH=1的溶液显酸性,离子之间发生氧化还原反应;
C.离子之间结合生成络离子;
D.由水电离的c(H+)=1×10-14mol?L-1的溶液,为酸或碱溶液.
解答:A.c(H+)/c(OH-)=1012的溶液中,c(H+)=0.1mol/L,溶液显酸性,该组离子之间不反应,能共存,故A正确;
B.pH=1的溶液显酸性,Fe2+、NO3-、H+离子之间发生氧化还原反应,则不能共存,故B错误;
C.c(Fe3+)=0.1mol?L-1的溶液中,Fe3+、SCN-离子之间结合生成络离子,则不能共存,故C错误;
D.由水电离的c(H+)=1×10-14mol?L-1的溶液,为酸或碱溶液,HCO3-既能与酸反应又能与碱反应,则一定不能共存,故D错误;
故选A.
点评:本题考查离子的共存,明确离子之间的反应及习题中的信息是解答本题的关键,注意选项B为解答的易错点,题目难度不大.
本题难度:一般