微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在120℃的条件下,总质量为2.1g的CO与H2的混合气体在足量的O2中充分燃烧,然后通过足量的Na2O2固体,固体增加的质量为
A.7.2g
B.4.2g
C.2.1g
D.3.6g
参考答案:C
本题解析:分析:利用差量法,根据化学方程式分析:
CO与H2在氧气中完全燃烧,生成CO2和H2O,生成的CO2和H2O再与Na2O2反应.
2CO+O2 2CO2,一氧化碳与二氧化碳物质的量相等,Na2O2与CO2反应2CO2+2Na2O2=2Na2CO3+O2,质量增重△m为2Na2CO3-2Na2O2=2CO,可知,反应后固体质量增加量为CO的质量;
2CO2,一氧化碳与二氧化碳物质的量相等,Na2O2与CO2反应2CO2+2Na2O2=2Na2CO3+O2,质量增重△m为2Na2CO3-2Na2O2=2CO,可知,反应后固体质量增加量为CO的质量;
2H2+O2 2H2O,生成的水与氢气物质的量相等,Na2O2与H2O反应2H2O+2Na2O2=4NaOH+O2,质量增重△m为2H2O-O2=2H2,可知,反应后固体增加的质量为氢气质量.
2H2O,生成的水与氢气物质的量相等,Na2O2与H2O反应2H2O+2Na2O2=4NaOH+O2,质量增重△m为2H2O-O2=2H2,可知,反应后固体增加的质量为氢气质量.
解答:2CO+O2 2CO2,一氧化碳与二氧化碳物质的量相等,Na2O2与CO2反应2CO2+2Na2O2=2Na2CO3+O2,
2CO2,一氧化碳与二氧化碳物质的量相等,Na2O2与CO2反应2CO2+2Na2O2=2Na2CO3+O2,
质量增重△m为2Na2CO3-2Na2O2=2CO,可知,反应后固体质量增加量为CO的质量;
2H2+O2 2H2O,生成的水与氢气物质的量相等,Na2O2与H2O反应2H2O+2Na2O2=4NaOH+O2,
2H2O,生成的水与氢气物质的量相等,Na2O2与H2O反应2H2O+2Na2O2=4NaOH+O2,
质量增重△m为2H2O-O2=2H2,可知,反应后固体增加的质量为氢气质量.
所以固体质量的增加量就是原混合气体的质量,为2.1g,
故选C.
点评:本题考查混合物的计算,难度中等,注意从CO2、H2O与Na2O2生成固体质量的变化分析规律,此为解答该题的关键.
本题难度:一般
2、选择题 在下列物质的溶液中分别加入一定量的Na2O2固体,不会出现浑浊现象的是
A.饱和Na2CO3溶液
B.Ca(HCO3)2稀溶液
C.Na2SO3稀溶液
D.饱和CaCl2溶液
参考答案:C
本题解析:分析:过氧化钠与水反应生成氢氧化钠和氧气,利用NaOH与选项中的物质的反应来分析是否生成沉淀,并注意对于饱和溶液来说,溶剂减少时会有溶质析出.
解答:A、过氧化钠固体与饱和Na2CO3溶液中的水反应,生成的NaOH不会与Na2CO3反应,但是溶液是饱和溶液,溶剂减少则会出现浑浊,故A错误;
B、过氧化钠固体与溶液中的水反应,生成的NaOH会与Ca(HCO3)2反应,生成碳酸钙白色沉淀,则出现浑浊,故B错误;
C、过氧化钠固体与Na2SO3溶液中的水反应,生成的NaOH不会与Na2SO3反应,此外,过氧化钠具有氧化性,可以将亚硫酸钠氧化为硫酸钠,均不会出现浑浊现象,故C正确;
D、过氧化钠固体与饱和氯化钙溶液中的水反应,生成的NaOH不会与氯化钙反应,但是溶液是饱和溶液,溶剂减少则会出现浑浊,故D错误.
故选C.
点评:本题考查过氧化钠与水的反应及复分解反应,明确物质之间的化学反应及反应中的现象是解答本题的关键,注意饱和溶液中溶剂和溶质的关系来解答.
本题难度:一般
3、选择题 某二价金属的碳酸盐和碳酸氢盐的混合物跟足量盐酸反应时消耗的H+和产生CO2的物质的量之比为5∶4,该混合物中碳酸盐和碳酸氢盐的物质的量之比为
A.1∶2
B.2∶3
C.3∶4
D.4∶5
参考答案:B
本题解析:设二价金属为M,混合物中碳酸盐(MCO3)和碳酸氢盐〔M(HCO3)2〕的物质的量分别为x和y,由题意可知:
![]()
![]()
![]()
![]()
![]()
![]()

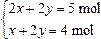 ?????解得
?????解得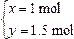 ????x∶y=2∶3
????x∶y=2∶3
本题难度:简单
4、选择题 下列不属于铵盐的共同性质的是
A.与烧碱反应共热产生氨气
B.都易溶于水
C.受热分解都产生氨气
D.都是晶体
参考答案:C
本题解析:试题分析:铵盐中都有铵根离子,与氢氧化钠共热都有氨气产生,铵盐都易溶于水,铵盐都是晶体,铵盐受热分解不一定产生氨气,如硝酸铵受到撞击分解生成氮气、氧气和水,D错误。
考点:铵盐的性质
点评:组成铵盐的酸若具有氧化性,则该铵盐受热分解一般不生成氨气。
本题难度:一般
5、选择题 将金属钾投入到氯化铁溶液中,产物是
A.OH
B.H2
C.e(OH)3
D.KCl
E.H2
F.e
G.KCl
H.HCl
I.Fe(OH)3
G.KCl
参考答案:B
本题解析:试题分析:钾是活泼的金属,极易和水反应生成氢氧化钾和氢气。然后生成的氢氧化钾再和氯化铁发生复分解反应生成氢氧化铁和氯化钾,答案选B。
考点:考查金属钾的化学性质
点评:该题是基础性试题的考查,学生主要是能够依据金属钠的化学性质进行类推即可。本题有利于培养学生的逻辑思维能力和知识的迁移能力。
本题难度:简单