微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某分子的球棍模型如图所示。已知分子中所有原子的最外层均达到8电子稳定结构,原子间以单键相连。下列有关说法中错误的是
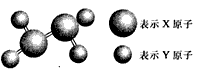 [???? ]
[???? ]
A.X原子可能为VA族元素
B.Y原子一定为IA族元素
C.该分子中,既含极性键,又含非极性键
D.从圆球的大小分析,该分子可能为N2F4
参考答案:B
本题解析:
本题难度:一般
2、选择题 下列关于晶体说法的正确组合是
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
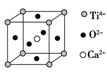
⑤CaTiO3晶体中(晶胞结构如上图所示)每个Ti4+和12个O2-紧邻
⑥SiO2晶体中每个硅原子与两个氧原子以共价键相结合
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
A.①②③⑥ ???????????? B.①②④
C.③⑤⑦??????????????????????????D.③⑤⑧
参考答案:D
本题解析:①错,如稀有气体不存在共价键;②错,如金属晶体是由金属阳离子和自由电子构成;③正确;④错,如氯化铵,既有离子键又有共价键;⑤正确;⑥错,SiO2晶体中每个硅原子与4个氧原子以共价键相结合;⑦错,分子间作用越大,物质的溶、沸点越高,但分子的稳定性与分子间作用力无关;⑧正确;
本题难度:一般
3、选择题
下列推测正确的是
A.XeF2分子中各原子均达到八电子结构
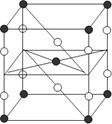
B.某种氟化氙的晶体结构单元如右图,可推知其化学式为XeF6
C.XeF4按已知方式水解,每生成4molXe,转移16mol电子
D.XeF2加入水中,在水分子作用下将重新生成Xe和F2
参考答案:C
本题解析:本题综合考查分子结构、晶体结构、氧化还原反应及氟气的性质,属较难题。Xe原子本身就是8电子结构,再与F原子结合,肯定就不再是了,所以A错;晶胞中Xe原子个数为:8×1/8+1=2,F原子个数为:8×1/4+2=4,故原子个数比Xe:F=1:2,其化学式为XeF2,B错;由题中化学方程式可知,生成3molO2失12mol电子,生成2molXeO3失4mol电子,生成4molXe得16mol电子,所以转移电子总数为12mol,故C正确;F2与水会剧烈反应,所以在溶液中不可能生成F2,D也错。易错警示:晶胞结构
本题难度:一般
4、填空题 在核电荷数为1―18的元素中,其单质属于金属晶体的有_______,金属中,密度最小的是_______,地壳中含量最多的金属元素是_______,熔点最低的是_______,既能与酸反应又能与碱反应的是_______,单质的还原性最强的是_______。
参考答案:Li、Be、Na、Mg、Al? Li? Al? Na? Be
本题解析:金属元素在元素周期表中的位置,一般可根据周期、族和主族序数来推断。凡是周期序数(原子的电子层数)大于主族序数(原子的最外层电子数)的元素,均为金属元素;若两序数相等的元素一般为既能与酸反应又能与碱反应的金属元素(H例外)。但其单质仍为金属晶体,如Be、Al;周期序数小于主族序数的元素一般为非金属元素。
本题难度:简单
5、填空题 下表列出了前20号元素中的某些元素性质的有关数据:
试回答下列问题:
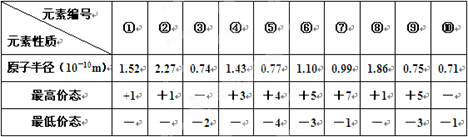
根据元素的主要化合价和原子半径可知,①~⑩分别是Cl、K、O、Al、C、P、Na、N、F。
(1)以上10种元素的原子中,失去核外第一个电子所需能量最少的是??????(填写编号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是(写分子式)?????????????。某元素R的原子半径为1.02×10-10m,该元素在周期表中位于?????????????;若物质Na2R2是一种含有非极性共价键的离子化合物,请你写出该化合物的电子式??????????????。
(3)元素⑤的某种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔融的②单质相互作用,形成某种青铜色的物质(其中的元素②用“●”表示),原子分布如图所示,该物质的化学式为???????????????。
参考答案:⑴ ②?⑵PCl3或CCl4?第三周期、ⅥA族 ![]()
本题解析:
试题分析:
(1)金属性越强,则第一电离能越小,所以10种元素的原子中,失去核外第一个电子所需能量最少的是K,即是②。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是PCl3或CCl4。同周期自左向右原子半径逐渐减小,自上而下原子半径逐渐最大,所以某元素R的原子半径为1.02×10-10m,该元素在周期表中位于第三周期、ⅥA族。该化合物的电子式类似于过氧化钠,所以电子式是 本题难度:一般
本题难度:一般