��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ����ʱ0.5L?2.0��10-4mol?L-1?BaCl2��Һ�У�����0.5L?1.0��10-3mol?L-1H2SO4��Һ���ܷ�����������������Ϻ���Һ��pHֵ������֪Ksp��BaSO4��=1.1��10-10?mol2?L-2��
2��ѡ���� ���ܵ����AB2������Һ�У�c��A2+��=x mol?L-1��c��B-��=y mol?L-1����Ksp��AB2��ֵΪ��������
A��
1
2
xy2
B��xy
C��xy2
D��4xy2
3��ѡ���� ��50 mL 0.018 mol/L AgNO3��Һ�м���50 mL 0. 02 mol/L���ᡣ��֪AgCl(s)���ܶȻ�����Ksp=1��10-10����Ϻ���Һ������仯���Բ��ơ�����˵������ȷ���� [???? ]
A����Ϻ���Һ�п϶��г�������
B���������ɺ���Һ��Ag+��Ũ��Ϊ10-5 mol/L
C���������ɺ���Һ��pH=2
D����Ϻ������¶ȣ���Һ��Ag+��Ũ������
4��ѡ���� �����£�����������ȷ����
A��pH��2��HA����Һ��pH��12��MOH����Һ������Ȼ�ϣ�c(H+) + c(M+)��c(OH��) + c(A��)
B������0.1mol/LNa2SO3��Һ��c(Na+)��2c(SO32��) + c(HSO3��) + 2c(H2SO3)
C����Ũ�ȡ�������Na2CO3��NaHCO3��ϣ�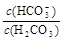 �� ��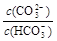
D��������AgCl�ֱ���룺��5mˮ����10mL0.2mol/LMgC12����20mL0.3mol/L�������ܽ������ͣ�c(Ag+)���٣��ڣ���
5������� �Ӻ�ˮ����ȡþ������������þ����Ҫ��Դ����������ȡþ�Ĺ������漰�ļ������ʵ��ܶȻ�����������ѧ��֪ʶ�ش����м������⣺
����
| CaCO3
| MgCO3
| Ca(OH)2
| Mg(OH)2
| �ܶȻ�
| 2.8��10�C9
| 6.8��10�C6
| 5.5��10�C6
| 1.8��10�C11
?
(1)�ڴӺ�ˮ����ȡþʱ�������õ�����(��Ҫ�ɷ���̼���)������Ϊ??????????(��ܡ����ܡ�)��������ĥ�ɷ�ĩֱ��Ͷ�뺣ˮ�У�������??????????????????????????????????���������ֱ��Ͷ�룬Ӧ���������δ�������д����ѧ����ʽ????????????????????????????????��
(2)ijͬѧ��ʵ����������ģ����������̣���ʵ������ʯ�ң����������ռ���棬����Ϊ??????????(����ԡ������ԡ�)�õ�Mg(OH)2���ڼ��Լ�ʱ��������Һ���뺣ˮ�У���˼����һ�£����ڵõ��Ļ����ϵ�м���������ռ���Һ���������??????????(��ܡ����ܡ�)��Mg2+ת��ΪMg(OH)2������������?????????????????????????????????????(�����ӷ���ʽ��ʾ)��
(3)��֪��ˮ��þ����Ũ��Ϊ1.8��10�C3mol��L�C1����Ҫʹþ���Ӳ�����������Һ��PH���ӦΪ??????????��
|
|