8.0
��ش��������⣺
��1���ڡ�����������У�Ϊ��߽������ʣ���ͨ����������衱�⣬���ɲ�ȡ�Ĵ�ʩ�� ��
��2������ͭп���к���������CuS��ZnS����H2SO4��������ZnS�����ܽ��CuS���ܣ�����ͬ�¶��£�Ksp(CuS) Ksp(ZnS)��ѡ�>����<����=������
��3������A���ʹ�����������е� ��
A��KMnO4 B������ C��HNO3 D��NaClO
��4�����������м��백ˮ��Ŀ���ǵ�����Һ��pH��pHӦ������ ��Χ֮�䡣
��5������B��ֱ���������ʣ���B�Ļ�ѧʽ�� ��
��6��������õ���Fe(OH)3����KClO��Һ�ڼ��Ի������������õ�һ�ָ�Ч�Ķ��ˮ����������K2FeO4��д���÷�Ӧ�����ӷ���ʽ ��
�ο��𰸣���1���ʵ������¶ȣ���������Ũ�ȡ�������ͭп�����ȣ�����2
���������
�����������1���ڡ�����������У�Ϊ��߽������ʣ���ͨ����������衱�⣬���ɲ�ȡ�Ĵ�ʩ���ʵ������¶Ȼ�������Ũ�ȡ�����������ͭп�����ȡ���2�����ʵ��ܽ��Խ���ڷ�ӦʱԽ�����з�Ӧ���������ͭп���к���������CuS��ZnS����H2SO4��������ZnS�����ܽ��CuS���ܣ�˵������ͬ�¶��£�Ksp(CuS) <Ksp(ZnS)����2������Fe2+��Zn2+�γɳ�������Һ��pH�ܽӽ����������룬�����ڹ�����Ҫ��Fe2+����ΪFe3+�����������������в��������µ��������ӣ����Լ��������A����ǿ�����ѡ����B����4�����������м��백ˮ��Ŀ���ǵ�����Һ��pH��pHӦ������Fe3+������ȫ��pH=3.2��Zn2+��ʼ�γɳ�����pH=6.2֮�䣬��3.2��pH<6.2����5�������ڲ��������м��������ᡢ��ˮ�����Բ����Ŀ�ֱ��������������B��(NH4)2SO4����6��������õ���Fe(OH)3����KClO��Һ�ڼ��Ի������������õ�һ�ָ�Ч�Ķ��ˮ����������K2FeO4������������ԭ��Ӧ�еĵ����غ㡢Ԫ�ص�ԭ�Ӹ����غ�ɵø÷�Ӧ�����ӷ���ʽ��2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O��
���㣺����Ӱ�컯ѧ��Ӧ���ʵ����ء������ܽ�ȴ�С�ıȽϡ��Լ���ѡ����ʹ�á���Ӧ������ѡ�����ʷ�Ӧ�����ַ���ʽ����д��֪ʶ��
�����Ѷȣ�����
2��ѡ���� ����HgS��������ˮ������Ȼ���гʺ��ɫ���������ͻ����ϡ�ӡ�༰����������ȡ�ij�¶�ʱ��HgS��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵����ȷ����
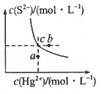
A����������Һ�м���������Һ������Ksp��С
B��ͼ��a���Ӧ���DZ�����Һ
C����c�����Һ�м���Hg(NO3)2����c(S2��)��С
D�������¶ȿ���ʵ��c�㵽b���ת��
�ο��𰸣�C
���������
���������ͼ�е����߱�ʾһ���¶���HgS�ı�����Һ������A��B����C��Hg2+������HgS���ܽ�ƽ�⣬����c(S2��)��С��C�ԣ�D�������¶ȣ����Ӿ���������
�����Ѷȣ�һ��
3��ѡ���� ���ܵ����AB2�ı�����Һ�У�[A2+]=xmol/L��[B-]=ymol/L����KspֵΪ��������
A��xy2
B��xy
C��xy2
D��4xy2
�ο��𰸣����ܵ����AB2�ĵ��뷽��ʽΪAB2��s��?A 2+��aq��
���������
�����Ѷȣ���
4������� ͭ���仯�����ڹ�ҵ�������ճ����������Ź㷺��Ӧ�á�
(1)?Li--CuO����ܷ�ӦΪ��2Li?+?CuO?=?Li2O?+?Cu���������ҺΪ��������л���Һ����ص�������ӦʽΪ?_____________��
(2)?Cu2O���ְ뵼����ϣ����ڼ�����Һ���õ�ⷨ��ȡ������ܷ�ӦʽΪ��2Cu?+?H2O Cu2O?+?H2����������ӦʽΪ_________��Cu2OͶ��ϡ�����У��õ���ɫ��Һ�ͺ�ɫ������д���÷�Ӧ�����ӷ���ʽ___________________�� Cu2O?+?H2����������ӦʽΪ_________��Cu2OͶ��ϡ�����У��õ���ɫ��Һ�ͺ�ɫ������д���÷�Ӧ�����ӷ���ʽ___________________��
(3)���Ȼ�����Һ��ʴӡˢ��·�ְ��ķ�Һ�У��������������ʵ���Ũ�ȵĶ���ֵ����ҺpH�ı仯����ͼ��ʾ(����Һ�н�������Ũ�ȡ�10�C5?mol��L?�C1ʱ������Ϊ������ȫ)��
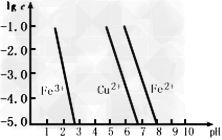
����ͼ��֪Fe(OH)2��Cu(OH)2���ܶȻ�Ksp[Fe(OH)2]________Ksp[Cu(OH)2](�>����<��)������Һ��Cu2+��Fe3+��Fe2+Ũ�Ⱦ�Ϊ0.1?mol/L��������ͨ�백��������Һ��pH?=?5.6ʱ����Һ�д��ڵĽ���������Ϊ________________��
(4)����ͭ�۶Ը�����淋��ȷֽ��д����ã�1?mol������立ֽ�ʱ������2?molˮ������1?mol�����⣬�������Ԫ�ؾ��γ���̬���ʡ��÷�Ӧ�Ļ�ѧ����ʽΪ_________________��1?mol������立ֽ���������������________mol��
�ο��𰸣�(1)CuO?�C?2e�C?+?2Li+?=?LiO?+?Cu
���������
�����Ѷȣ�һ��
5��ѡ���� ����ʱ��CaCO3��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪CaCO3���ܶȻ������£�Ϊ2.8��10-9������˵���в���ȷ����

A��x����ֵΪ2��10-5
B��c��ʱ��CaCO3����
C����������ˮ��ʹ��Һ��d���� a��
D��b����d���Ӧ���ܶȻ����
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
|