微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,将稀NaOH溶液与稀CH3COOH溶液混合,不可能出现的结果是??? (??? )
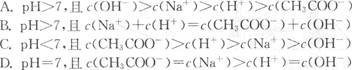
参考答案:A
本题解析:溶液中肯定c(Na+)>c(OH-)
本题难度:一般
2、填空题 一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如下图所示,
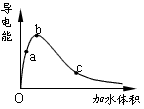
(1)O点导电能力为0的理由是___________________________________
(2)a、b、c三点溶液的c(H+)由小到大的顺序是___________________________________
(3)a、b、c三点醋酸的电离程度最大的是__________________________________
(4)要使c点c(CH3COO- )增大,c(H+)减少,可采取的措施是(至少写出三种方法)①_____________ ②___________________③__________________________
参考答案:
(1)在O点醋酸未电离,无自由离子存在
(2)
本题解析:
本题难度:一般
3、选择题 对于常温下0.1 mol・L-1氨水和0.1 mol・L-1醋酸,下列说法正确的是
A.0.1 mol・L-1氨水,溶液的pH=13
B.0.1 mol・L-1氨水加水稀释,溶液中c(H+)和c(OH-)都减小
C.0.1 mol・L-1醋酸溶液中:c(H+)=c(CH3COO-)
D.0.1 mol・L-1醋酸与0.1 mol・L-1NaOH溶液等体积混合所得溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
参考答案:D
本题解析:
试题分析:A、氨水属于弱电解质,部分电离NH3 NH4++OH―,故常温下0.1 mol・L-1氨水,溶液的pH<13,A错误;B、氨水加水稀释,碱性减弱,c(OH-)减小,Kw不变,c(H+)增大,B错误;C、0.1 mol・L-1醋酸溶液中存在电荷守恒c(H+)=c(CH3COO-)+c(OH-
NH4++OH―,故常温下0.1 mol・L-1氨水,溶液的pH<13,A错误;B、氨水加水稀释,碱性减弱,c(OH-)减小,Kw不变,c(H+)增大,B错误;C、0.1 mol・L-1醋酸溶液中存在电荷守恒c(H+)=c(CH3COO-)+c(OH-
本题难度:一般
4、选择题 氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是
A.HCN易溶于水
B.HCN溶液能导电
C.1mol/L氢氰酸溶液的pH约为3
D.10 mL1 mol・L-1HCN恰好与10 mL 1 mol・L-1 NaOH溶液完全反应
参考答案:C
本题解析:
试题分析:能溶于水的物质不一定是弱电解质如硝酸故A选项是错误的。能导电不能说明氢氰酸是弱电解质。弱电解质与强电解质的本质区别是,强电解质在水溶液中能完全电离,而若电解质不可以。C选项若氢氰酸是强酸则PH为0小于3,所以氢氰酸为弱酸。所以答案选C,而D选项无论氢氰酸是强酸还是弱酸都恰好能完全发生反应。
本题难度:简单
5、填空题 (17分)二氧化硫为重要的含硫化合物,是形成酸雨的主要污染物之一。
(1)在实验室中,若用70%的硫酸溶液和亚硫酸钠粉末反应制取二氧化硫,并要求方便控制反应速率,可选用下图所示气体发生装置中的_____(填下列序号字母)。

(2)SO2经催化氧化可生成SO3,该反应的热化学方程式为:2SO2(g)+O2(g) 2SO3(g) △H="a" kJ・mol-1
2SO3(g) △H="a" kJ・mol-1
在T1℃时,将2 mol SO2、1mol O2充入容积为2 L的密闭容器A中,充分反应并达到平衡,此过程中放出热量98.3 kJ,测得SO2的平衡转化率为50%,则a=_____,T1℃时,上述反应的平衡常数K1=____L・mol-1。若将初始温度为T1℃的2 mol SO2和1 molO2充入容积为2 L的绝热密闭容器B中,充分反应,在T2℃时达到平衡,在此温度时上述反应的平衡常数为K2。则K1______K2(填“>”、“<”或“=”)。
(3)某热电厂上空大气中所含二氧化硫严重超标,现对该区域雨水样品进行探究。首先用pH试纸测定雨水样品的pH,操作方法为___________________________,测得样品pH约为3;为进一步探究由SO3所形成酸雨的性质,将一定量的SO2通入蒸馏水中,配成pH为3的溶液,然后将溶液分为A、B两份,向A中加入适量的NaOH固体,使溶液恰好呈中性(不考虑氧化性物质和其它酸性物质的影响),则此中性溶液中离子的浓度间存在的关系式为:[Na+]=______________;将溶液B久置于空气中,与久置前相比,久置后的溶液B中水的电离程度将__________(填“增大”、“减小”或“不变”)。
(4)工业上常用如下图所示的流程处理工业尾气中的SO2:
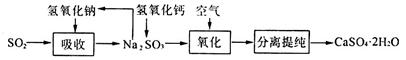
上述流程中有一种物质可以再生循环利用,该物质再生的化学方程式为___________________.
参考答案:(1)(2分)a
(2)(6分)-196.6;4;<<
本题解析:
试题分析:(1)在实验室中,若用70%的硫酸溶液和亚硫酸钠粉末反应制取二氧化硫,并要求方便控制反应速率,可选用下图所示气体发生装置中的a。(2)根据题意知,在T1℃时,将2 mol SO2、1mol O2充入容积为2 L的密闭容器A中,充分反应并达到平衡,此过程中放出热量98.3 kJ,测得SO2的平衡转化率为50%,即1molSO2参加反应放出热量98.3 kJ,该反应的热化学方程式为:2SO2(g)+O2(g) 2SO3(g) △H=-196.6;4 kJ・mol-1,则a=-196.6;4;T1℃时,反应达平衡时各物质的浓度分别为:c(SO2)="0.5" mol/L 、c(O2)=" 0.25" mol/L、c(SO3)=0.5mol/L,代入平衡常数表达式计算,上述反应的平衡常数K1=4L・mol-1。若将初始温度为T1℃的2 mol SO2和1 molO2充入容积为2 L的绝热密闭容器B中,充分反应,2SO2(g)+O2(g)
2SO3(g) △H=-196.6;4 kJ・mol-1,则a=-196.6;4;T1℃时,反应达平衡时各物质的浓度分别为:c(SO2)="0.5" mol/L 、c(O2)=" 0.25" mol/L、c(SO3)=0.5mol/L,代入平衡常数表达式计算,上述反应的平衡常数K1=4L・mol-1。若将初始温度为T1℃的2 mol SO2和1 molO2充入容积为2 L的绝热密闭容器B中,充分反应,2SO2(g)+O2(g) 2SO3(g) △H=―196.6;4 kJ・mol-1,为放热反应,温度:T2>T1,升高温度平衡逆向移动,平衡常数减小,则K1<K2。(3)用pH试纸测定雨水样品的pH,操作方法为取一条试纸放在干燥洁净的表面皿(或玻璃片)上,用干燥洁净的玻璃棒蘸取雨水样品点在试纸上,待变色后立即对照标准比色卡读数;向二氧化硫水溶液中加氢氧化钠固体使溶液恰好呈中性所得溶液为亚硫酸钠和亚硫酸氢钠的混合液,根据电荷守恒知[H+]+[Na+]=2[SO32-]+[HSO3-] +[OH-],又[H+]=2[SO32-]+[HSO3-],则此中性溶液中离子的浓度间存在的关系式为:[Na+]=2[SO32-]+[HSO3-];将二氧化硫水溶液久置于空气中发生反应2H2SO3+O2
2SO3(g) △H=―196.6;4 kJ・mol-1,为放热反应,温度:T2>T1,升高温度平衡逆向移动,平衡常数减小,则K1<K2。(3)用pH试纸测定雨水样品的pH,操作方法为取一条试纸放在干燥洁净的表面皿(或玻璃片)上,用干燥洁净的玻璃棒蘸取雨水样品点在试纸上,待变色后立即对照标准比色卡读数;向二氧化硫水溶液中加氢氧化钠固体使溶液恰好呈中性所得溶液为亚硫酸钠和亚硫酸氢钠的混合液,根据电荷守恒知[H+]+[Na+]=2[SO32-]+[HSO3-] +[OH-],又[H+]=2[SO32-]+[HSO3-],则此中性溶液中离子的浓度间存在的关系式为:[Na+]=2[SO32-]+[HSO3-];将二氧化硫水溶液久置于空气中发生反应2H2SO3+O2 2H2SO4,溶液的酸性增强,水的电离程度将减小。(4)根据题给流程判断可以再生循环利用的物质为氢氧化钠,再生的化学方程式为Na2SO3+Ca(OH)2=CaSO3↓+2NaOH。
2H2SO4,溶液的酸性增强,水的电离程度将减小。(4)根据题给流程判断可以再生循环利用的物质为氢氧化钠,再生的化学方程式为Na2SO3+Ca(OH)2=CaSO3↓+2NaOH。
考点:考查二氧化硫的性质,化学实验基本操作,化学平衡,盐类的水解和化学方程式的书写。
本题难度:困难