微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 “1mol/L的Na2SO4溶液”的含义是[???? ]
A.1L水中有1mol Na2SO4
B.1L溶液中含有142g Na2SO4
C.SO42-的物质的量浓度为2mol/L
D.1LNa2SO4溶液中含有Na+ 1mol
参考答案:B
本题解析:
本题难度:简单
2、选择题 设NA为阿伏加德罗常数的值,下列有关叙述不正确的是
A.标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为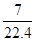 NA
NA
B.1 mol甲基(―CH3)所含的电子总数为7NA
C.0.5 mol 1, 3-丁二烯分子中含有C=C双键数为 NA
D.1 mol碳正离子(CH3+)所含的电子总数为8NA
参考答案:AB
本题解析:标准状况下庚烷不是气体,A不正确。甲基中的电子数是6+1×3=9,B错误。1, 3-丁二烯分子中含有2个碳碳双键,C正确。碳正离子含有的电子数是6+1×3-1=8,D正确。所以答案选AB。
本题难度:一般
3、选择题 由氧化铜和氧化铁组成的混合物a g,加入2 mol・L-1的稀硫酸溶液50 mL,恰好完全溶解,若将a g的该混合物在过量的CO气流中加热充分反应,冷却后剩余固体的质量为
A.1.6a g
B.(a-1.6) g
C.(a-3.2) g
D.无法计算
参考答案:B
本题解析:
试题分析:加入2mol/L的H2SO4溶液50 mL恰好完全反应,此时生成水、硫酸铜和硫酸铁。硫酸是0.1mol,则根据氢原子守恒可知生成0.1mol水,所以根据氧原子守恒可知混合物中氧原子的物质的量是0.1mol,质量是1.6g,所以根据原子守恒可知若将a g的该混合物在过量的CO气流中加热充分反应,冷却后剩余固体的质量为ag―1.6g,答案选B。
考点:考查混合物的有关计算
本题难度:一般
4、选择题 配制一定物质的量浓渡的NaOH溶液时,使所配制的溶液浓度偏小的操作是( )
①将NaOH固体放在纸上称量,再转移到烧杯中溶解
②烧杯中NaOH溶液移入容量瓶后没有洗涤烧杯
③实验用的容量瓶洗净后末干燥,里面含有少量水
④读取容量瓶液面时采用俯视.
A.①②
B.③④
C.①③
D.②④
参考答案:①将NaOH固体放在纸上称量,再转移到烧杯中溶解,导致氢氧化
本题解析:
本题难度:一般
5、简答题 用18.4mol/L的浓硫酸稀释成0.92mol/L的稀硫酸100ml,回答下列问题:
(1)
| 应取浓硫酸的体积/ml | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器
(2)配制操作可分解成如下几步:
A向容量瓶中注入少量蒸馏水,检查容量瓶是否漏水
B用少量蒸馏水洗涤烧杯,将溶液注入容量瓶,并重复操作两次
C将已冷却的硫酸注入容量瓶中
D根据计算,用量筒量取一定体积的浓硫酸
E将浓硫酸沿烧杯壁慢慢注入盛有蒸馏水的小烧杯中,并不断用玻璃棒搅拌
F盖上容量瓶塞子,振荡,摇匀,装瓶
G用胶头滴管继续加蒸馏水,使溶液凹面恰好与刻度相切
H继续往容量瓶中小心地加蒸馏水,使液面接近刻度线
正确的操作顺序是:A______F
(3)下列操作结果,使溶液物质的量浓度偏低的是______
A没有将洗涤液转移到容量瓶中
B容量瓶洗净后未经干燥处理
C转移过程中有少量的溶液溅出
D摇匀后立即观察,发现溶液未达刻度线,没有再用滴管加几滴蒸馏水至刻度线.
参考答案:(1)配制100mL 0.92mol/L的稀硫酸,需要选用1
本题解析:
本题难度:一般
|