微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 在水的电离平衡中,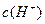 和
和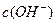 的关系如下图所示:
的关系如下图所示:
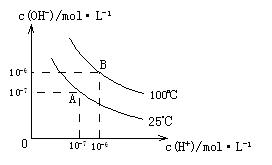
(1)A点水的离子积为1×10-14,B点水的离子积为??????????。造成水的离子积变化的原因是??????????????????????????????????????????????????。
(2)25℃时,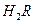 在水溶液中的电离方程式为:
在水溶液中的电离方程式为:
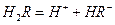 ,
,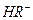

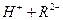 。
。
① 0.1 mol/L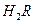 溶液的pH????????1(填“>”、“<”或“=”)。
溶液的pH????????1(填“>”、“<”或“=”)。
②在0.1 mol/L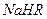 溶液中,各离子浓度由大到小的顺序是:
溶液中,各离子浓度由大到小的顺序是:
????????????????????????????????????????????????????????。
(3)100℃时,0.01 mol/L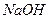 溶液的pH = ????????????。
溶液的pH = ????????????。
(4)100℃时,将pH =8的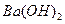 溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则
溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则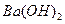 溶液与盐酸的体积比为???????????。
溶液与盐酸的体积比为???????????。
参考答案:(1) 本题解析:略
本题解析:略
本题难度:简单
2、选择题 一定温度下,反应2SO2 + O2 2SO3达到平衡时,n(SO2)∶n(O2)∶n(SO3) =2∶3∶4。缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是[???? ]
2SO3达到平衡时,n(SO2)∶n(O2)∶n(SO3) =2∶3∶4。缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是[???? ]
A.0.4mol
B.0.6mol?
C.0.8mol
D.1.2mol
参考答案:A
本题解析:
本题难度:一般
3、选择题 等物质的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g)=2Z(g)+W(s)ΔH<0,下列叙述正确的是(?)
A.达到平衡后,降低温度,正向反应速率减小的倍数大于逆向反应速率减小的倍数
B.达到平衡后,升高温度或增大压强都有利于该反应平衡向逆反应方向移动
C.达到平衡时,反应速率v正(X)=2v逆(Z)
D.平衡常数K值越大,X的转化率越大
参考答案:D
本题解析:A错,该反应正反应方向为放热反应,降低温度,平衡向正反应方向移动,即正反应速率大于逆反应速率,减小倍数更小;B错,升高温度该反应向逆反应方向移动,但增大压强,由于反应为等体积反应平衡不移动;C错,达到平衡时,反应速率2v正(X)=v逆(Z);D正确;
本题难度:一般
4、选择题 在一密闭烧瓶中,在25℃时存在着平衡2NO2 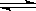 ?N2O4,△H<0。把烧瓶置于100℃的水中,则下列几项性质中不会改变的是?(???)
?N2O4,△H<0。把烧瓶置于100℃的水中,则下列几项性质中不会改变的是?(???)
①颜色?②平均相对分子质量?③质量?④压强?⑤密度
A.①和③
B.②和④
C.④和⑤
D.③和⑤
参考答案:D
本题解析:温度升高向逆向进行,颜色变深,物质的量减小质量不变,摩尔质量变大。质量不变体积不变,密度不变,压强不变。
本题难度:一般
5、选择题 向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s) bZ(g);△H<0。如图是容器中X、Z的物质的量浓度随时间变化的曲线。下列说法正确的是(???)
bZ(g);△H<0。如图是容器中X、Z的物质的量浓度随时间变化的曲线。下列说法正确的是(???)
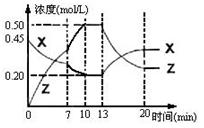
A.用Y表示0~10min内该反应的平均速率为0.05mol/(L・min)
B.根据上图可求得方程式中a:b=2:1
 0~10min容器内气体的压强逐渐增大
0~10min容器内气体的压强逐渐增大
D.第13min时曲线变化的原因可能是增加了Z的量
参考答案:C
本题解析:略
本题难度:简单