微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 有Na2SO4和Na2CO3混和溶液10.0毫升,加入足量BaCl2溶液,充分反应后,经过滤、洗涤和烘干,得到白色沉淀1.451克.将沉淀与过量盐酸反应,得到112毫升CO2气体(标准状况).求原混和溶液中Na2SO4和Na2CO3的物质的量浓度.
参考答案: 本题解析:略
本题解析:略
本题难度:一般
2、计算题 agNa2CO3和NaHCO3混合物加热至质量减少到bg,则混合物 中NaHCO3的质量分数为:????。
中NaHCO3的质量分数为:????。
参考答案: 本题解析:解:设NaHCO3的质量为x
本题解析:解:设NaHCO3的质量为x
2NaHCO3====Na2CO3+H2+CO2↑????????????????? △m
168g??????? 106g?????????????????????? 168g-106g=62g
x??????????????????????????????????????(a-b)g
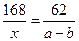 本题难度:简单
本题难度:简单
3、选择题 取a g某物质A,在氧气中完全燃烧,使燃烧产物跟足量过氧化钠反应,反应后固体的质量增加了b g。若b>a,则A为(??? )
A.H2
B.CO
C.C12H22O11
D.C6H12O6
参考答案:C
本题解析:本题是在计算的背景下对过氧化钠性质的考查,同时考查归纳综合能力。若按上述过程进行实验,发生反应:
(1)2H2+O2====2H2O;
2Na2O2+2H2O====4Na2OH+O2↑
连续反应,叠加方程式可知:
H2+Na2O2====2NaOH
(2)2CO+O2====2CO2;
2Na2O2+2CO2====2Na2CO3+O2;
连续反应,叠加方程式可知:CO+Na2O2====Na2CO3;
由此可知H2、CO、O2在Na2O2中不耗O2,固体
本题难度:简单
4、填空题 运用比较方法是化学科学中研究物质性质的基本方法之一,请运用比较法解答下题:过氧化钠几乎可与所有的常见气态非金属氧化物反应。如:2Na2O2+2CO2=2Na2CO3+O2↑,Na2O2+2CO=Na2CO3
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式:__________________。_________________。
(2)通过比较可知,当非金属元素处于__________价时,其氧化物与过氧化钠反应有O2生成。
参考答案:(1)2Na2O2+2SO3==2Na2SO4+O2↑;Na
本题解析:
本题难度:一般
5、实验题 我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他利用NaHCO3、NaCl、NH4C1等物质溶解度的差异,以食盐、氨气为原料先制得NaHCO3,进而生产出纯碱。下面是在实验室中模拟“侯氏制碱法”中制取NaHCO3的实验步骤:
第一步:连接好装置图(如下),检查气密性,在仪器内装入药品。
第二步:先让一装置发生反应,直到产生的气体不能再在C中溶解时,再通入另一装置中产生的气体,片刻后C中出现固体,继续向C中通入两种气体,直到不再有固体产生。
第三步:过滤C中所得的混合物,得到NaHCO3固体。
第四步:向滤液中加入适量的NaCl粉末,有NH4Cl晶体析出。
请回答下列问题:
(1)装置的连接顺序是:(a)接(? )(? )接(? );(b)接(? )。
(2)A中常选用的固体为?????????????;D中应选用的液体为????????????;B中发生反应的化学方程式为???????????????????????????????????????。
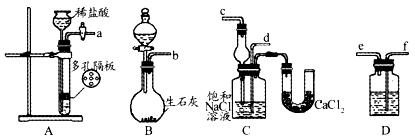
(3)第二步中必须让?????????装置先发生反应。
(4)C中用球形干燥管而不用直导管,其作用是????????????????????,C中广口瓶内发生反应的化学方程式为????????????????????????????????????????。
(5)第四步中分离出NH4Cl晶体的操作是????????????;其所得的NH4Cl晶体中常含有少量的NaCl和NaHCO3 (约占5%~8%),请设计一个简单的实验证明所得固体的成分大部分是NH4Cl,简要写出操作和现象:?????????????????????????????????????????????????。
参考答案:(1)f? e? d? c? (2)块状石灰石??饱和NaH
本题解析:(1)f? e? d? c? (2)块状石灰石??饱和NaHCO3溶液 CaO+NH3・H2O==Ca(OH)2+NH3↑(其他合理答案也可)? (3)B? (4)防倒吸CO2+NH3+NaCl+H2O==NaHCO3↓+NH4Cl? (5)过滤?取少量固体放入试管中加热;固体大部分消失,在试管口又有较多的固体凝结(其他合理答案均可)
本题难度:一般