微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 硼有两种天然同位素10B和11B,硼元素的相对原子质量为10.8,则10B与11B的物质的量之比为(??)
A.1∶4
B.1∶2
C.1∶1
D.1∶3
参考答案:A
本题解析:
本题难度:一般
2、选择题 在元素周期表的金属元素和非金属元素交界处,最容易找到的材料是
A.制半导体的材料
B.耐高温、耐腐蚀的合金材料
C.制农药的材料
D.制催化剂的材料
参考答案:A
本题解析:
本题难度:简单
3、填空题 A、B、R、D、E、F是六种原子序数依次增大的短周期元素, 其中有两种非金属元素位于同一主族。已知A、B、D均能与R形成原子(或离子)个数不同的几种常见化合物。请回答下列有关问题。
(1)仅由上述信息就可以确定的元素(写出代号与元素符号)是________________,若X、Y是D、F形成的最高价氧化物对应的水化物,浓度均为0.1mol/L的X、Y溶液的pH之和为14,则X、Y的晶体熔点相对高低为(写化学式)______???______
(2) A与B、E均可形成正四面体构型的气态分子Q、P,又知P的燃烧热为1430kJ/mol,则其燃烧的热化学方程式___________???????????????????_________
(3) 上述六种元素间能形成多种常见二元化合物,其中存在两类化学键的物质的电子式为_____??__(写一种即可)
(4) R能形成多种单质,如R2、R3,研究表明,新近制得的一种组成为R4的分子中,每个R原子均与另外两个R原子各形成一个键,下列有关R4的说法中正确的是__??_____
①R4与R3、R2互为同位素?????????????????②R4不能与A、B、D的单质反应
③R4中各原子最外电子层均为8电子结构???④R4是一种新型化合物
参考答案:(1)R:O,NaOH >HClO4;
(2)S
本题解析:
本题难度:简单
4、选择题 下列关于化学观或化学研究方法的叙述中,错误的是(???? )
A.在化工生产中应遵循“绿色化学”的思想
B.控制实验条件可以改变化学反应的限度和速率
C.在元素周期表的金属和非金属分界线附近寻找半导体材料
D.根据元素周期律,由HClO4可以类推出氟元索也存在最高价氧化物的水化物HFO4
参考答案:D
本题解析:
本题难度:一般
5、实验题 某研究性学习小组进行如下探究活动:
实验目的:探究Cl2、Br2、I2的氧化性强弱。
查阅资料:①常温下,高锰酸钾与浓盐酸反应产生氯气;②溴单质易挥发,碘单质易生华;③淀粉溶液遇到碘单质变蓝色;
④溴、碘在不同溶剂中所形成溶液(从稀到浓)的颜色变化如图所示。
?
| 水
| 四氯化碳
|
溴
| 黄→棕
| 橙→橙红
|
碘
| 深黄→褐
| 紫→深紫
??实验方案:该小组设计下图所示装置实验(夹持仪器已略去,装置气密性完好)
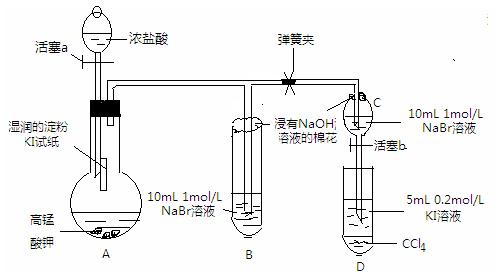 ? ?
实验过程:
Ⅰ 先打开弹簧夹,再打开活塞a,滴加浓盐酸
Ⅱ 当B和C中的溶液都变黄时,加紧弹簧夹
Ⅲ 当B中的溶液由黄色变为棕色时,关闭活塞a
Ⅳ … …
回答以下问题:
⑴验证氯气的氧化性强于碘的实验现象是??????????,写出该反应的化学方程式??????????????????????????????????;
⑵为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是??????????????,写出
该反应的离子方程式???????????????????????;
⑶由实验得到的氯、溴、碘单质的氧化性由强到弱的顺序为????????????;
⑷你认为实验中为什么要加过程Ⅲ这一步操作,请简述个人观点??????????????
参考答案:
 本题解析: 本题解析:
本题难度:一般
|