��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ij��Һ����Fe3+��Al3+��Ba2+��Ag+��K+���������ӣ����ù�����H2SO4��NaOH��NH3��H2O��NaCl������Һ����ͼ��ʾ�IJ���ֿ��������ӡ������ж���ȷ����
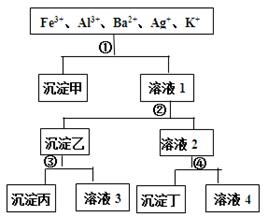
A�����������������������������Ļ����
B����Һ3�к���Al3+
C����Һ4�������������ӣ��ֱ���H+��Na+��K+
D���Լ�����NaCl���Լ�����H2SO4
�ο��𰸣�D
���������
�����������ΪNaCl����Ag+ת��Ϊ��������Ϊ��ˮ��������ΪFe(OH)3��Al(OH)3�����������NaOH��Al(OH)3ת��ΪNaAlO2����Һ3��������ΪFe(OH)3������Һ2��Ba2+��K+���м���H2SO4�����ɳ�����BaSO4��A��������ΪFe(OH)3��Al(OH)3������B����Һ3ΪNaAlO2������C����Һ4�л���笠����ӣ�����
�����Ѷȣ�һ��
2������� ����һ������Һ��ֻ���ܺ����±��е�����������(���ڵ����Ӿ�����)��
������
| K����NH4+��H����Ba2��
|
������
| Cl����CO32-��SO42-��OH��
��ȡ��������������Һ��100 mL���ֱ��������ʵ�飺
�ٵ�һ�ݼ���AgNO3��Һ�г���������
�ڵڶ��ݼ�������NaOH��Һ���Ⱥ��ռ�������0.04 mol��
�۵����ݼ�������BaCl2��Һ�ø������6.27 g������������ϴ�ӣ������������Ϊ2��33 g��
��ش��������⣺
(1)100 mL��Һ��c(SO42-)��_____________________��
(2)�ڶ��ݼ���NaOH��Һ������������ӷ���ʽ_____________________
(3)6��27 g�����ijɷ���_____________________ (�û�ѧʽ��ʾ)��
(4)����������Һ�г�SO42-���⣬һ���������ڵ�������_____________________
�ο��𰸣���1��0.1 mol��L��1
��2��NH4++OH��<
����������������⣬Ba2+��SO42-���ɷ������ӷ�Ӧ����BaSO4������������߲��ܴ������森Ba2+��CO32-�ɷ������ӷ�Ӧ����BaCO3�������������Ҳ���ܴ�������
��һ�ݼ���AgNO3��Һ�г������������ܷ���Cl-+Ag+�TAgCl����CO32-+2Ag+�TAg2CO3����SO42-+2Ag+�TAg2SO4�������Կ��ܺ���Cl-��CO32-��SO42-
�ڶ��ݼ�����NaOH��Һ���Ⱥ��ռ�������0.04mol���ܺ�NaOH��Һ���Ȳ��������ֻ����NH4+����û�г�������˵��һ��������Mg2+
�����Ѷȣ���
3��ѡ���� �ں���4 mol HCl��1 mol MgSO4�Ļ����Һ����μ���Ba(OH)2��Һ�������ij�������m�����Ba(OH)2���ʵ���n֮��Ĺ�ϵ����ͼ������˵����ȷ����(??? )

A��a��bʱ�ij����ijɷ�ΪBaSO4��Mg(OH)2
B��b��cʱ���������ӷ�ӦΪ��H+ + OH�� �� H2O
C��c��dʱ���ӵ����ʵ�����Ba2+���ܴ���Cl��
D��d��eʱ���ӵ����ʵ�����Ba2+һ������OH��
�ο��𰸣�B
���������
����������������Һ�м�Ba(OH)2��Һ����ʼ�η����ķ�ӦΪBa2++SO42- +2H+ + 2OH�� = BaSO4��+ 2H2O��ͼ��Ϊa-b�Σ���SO42- ����ȫ����ʱ������2mol H+?�����Լ����μ�Ba(OH)2��Һ�������ķ�ӦΪH+ + OH�� = H2O������������ͼ��Ϊb-c�Σ��ý�����Ba(OH)2 1mol���ټ����μ�Ba(OH)2��Һ��������ӦΪMg2++ 2OH�� = Mg(OH)2�������Գ��������࣬ͼ��Ϊc-d�Σ���þ������ȫ��������������������࣬ͼ��
�����Ѷȣ�һ��
4��ѡ���� ij��Һ�к���NO3-��SiO32-��AlO2-��S2-��4�����ӣ��������м��������������Һ���Ȳ����裬�ټ������������������Һ������Һ��������Ŀ�������ٵ���[???? ]
A��ֻ��S2-
B��S2-��NO3-
C��SiO32-��S2-��NO3-
D���������Ӷ�����
�ο��𰸣�B
���������
�����Ѷȣ���
5��ѡ���� ���з�Ӧ�У����������ӷ�Ӧ��������������ԭ��Ӧ����?????
A��H2+O2
B��CO+CuO
C��Zn+H2SO4
D��NaOH+CO2
�ο��𰸣�C
�����������
�����Ѷȣ���
|