微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 以2-溴丙烷为原料制取1,2-丙二醇,需要经过的反应是
A.加成―消去一取代
B.取代一消去―加成
C.消去―取代一加成
D.消去―加成―取代
参考答案:D
本题解析:试题分析:由2-溴丙烷制取少量的1,2-丙二醇,可用逆推法判断,即CH3CHOHCH2OH CH3CHBrCH2Br
CH3CHBrCH2Br CH3CH=CH2
CH3CH=CH2 CH3CHBrCH3,则2-溴丙烷应首先发生消去反应生成CH3CH=CH2,CH3CH=CH2发生加成反应生成CH3CHBrCH2Br,CH3CHBrCH2Br发生水解反应可生成1,2-丙二醇,答案选D。
CH3CHBrCH3,则2-溴丙烷应首先发生消去反应生成CH3CH=CH2,CH3CH=CH2发生加成反应生成CH3CHBrCH2Br,CH3CHBrCH2Br发生水解反应可生成1,2-丙二醇,答案选D。
考点:考查有机物合成的方案的设计
点评:该题是高考中的常见题型,属于中等难度的试题,侧重对学生基础知识的巩固,旨在培养学生分析、归纳、总结问题的能力。注意把握有机物官能团的变化,为解答该题的关键。
本题难度:简单
2、选择题 向FeCl3和BaCl2的酸性混合溶液中,通入SO2气体,有白色沉淀生成。此沉淀是( )
A.BaSO4
B.FeS
C.BaSO3
D.S
参考答案:A
本题解析:
试题分析:向FeCl3和BaCl2的酸性混合溶液中通入SO2气体,发生2Fe3++SO2+2H2O
本题难度:一般
3、选择题 影响活化分子的百分数的因素有
①温度②浓度③压强④催化剂⑤接触面积
A.①②
B.①②③④
C.①④
D.②④
参考答案:C
本题解析:只有温度和催化剂才能增大活化分子的百分数,所以答案选C。
本题难度:简单
4、填空题 (1)黄铁矿(FeS2)是制造硫酸的矿物原料,反应历程为FeS2→SO2→SO3→H2SO 4,请写出
SO2制备SO3反应的化学方程式,并用双线桥标出电子转移的方向和数目 ;
(2)下列酸在与黄铁矿(FeS2)发生反应时,其中S或N元素的化合价不会发生变化的是 ;
a.稀硫酸 b.稀硝酸 c.浓硫酸 d.浓硝酸
(3)从矿物学资料查得,自然界存在反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,
该反应的氧化剂为 ,反应中转移的电子数为 NA;
(4)将(2)中反应的产物溶于水后过滤(Cu2S不溶于水和稀酸),再将滤液滴入用硫酸酸化的高锰酸钾溶液中发现溶液褪色,已知反应后锰元素呈+2价,请写出反应的化学方程式 。
参考答案:
(1) 本题解析:
本题解析:
试题分析:(1)SO2在催化剂下转化为SO3即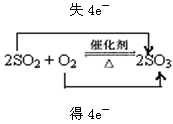
(2)a、稀硫酸是非氧化性酸,与金属反应时,氢离子显示氧化性,氧化金属,S元素价态不变,故a正确;b、稀硝酸为氧化性酸,与金属反应时,硝酸根显示氧化性,氧化金属,N元素被还原,故b错误;c、浓硫酸是氧化性酸,加热与金属反应时,硫酸根显示氧化性,氧化金属,S元素被还原,故c错误;d、浓硝酸为氧化性酸,与金属反应时,硝酸根显示氧化性,氧化金属,N元素被还原,故d错误;(3)氧化剂发生还原反应化合价降低,14CuSO4+5FeS2+12H2O
本题难度:一般
5、选择题 下列离子中能使纯水的电离程度减小的是
A.F―
B.HCO3―
C.Cl―
D.HCOOH
参考答案:D
本题解析:要使水的电离程度减小,可以加酸或者加碱,所以应该选择D.另外F-水解,使水电离程度增大,碳酸氢根离子水解也使水的电离程度增大,氯离子不会引起水电离程度的变化.
本题难度:简单