微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得溶液中加入0.1molCu(OH) 2后恰好恢复到电解前的浓度和pH。则电解过程中转移的电子数为
A.0.1mol
B.0.2mol
C.0.3mol
D.0.4mol
参考答案:D
本题解析:
试题分析:Cu(OH)2从组成上可看成CuO?H2O,加入0.1 mol Cu(OH)2后恰好恢复到电解前的浓度和pH,即电解生成了0.1 mol H2SO4,并消耗0.1 mol H2O,由电解的总反应式为:
2H2O+2CuSO4 2Cu+O2↑+2H2SO4 ??????转移电子
2Cu+O2↑+2H2SO4 ??????转移电子
2mo
本题难度:一般
2、实验题 已知pH为4-5的条件下,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(n)以及电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,过程如下
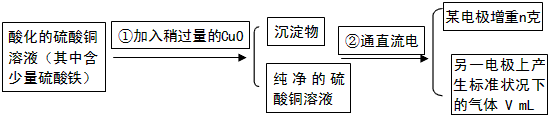
回答下列问题:
(1)加入CuO的作用是_______________________。
(2)步骤②中所用的部分仪器如下图所示,则A、B分别连直流电源的__________和__________极(填“正”或“负”)。
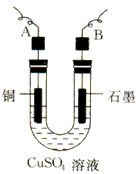
(3)电解开始后,在U形管中可以观察到的现象有:________________________
电解的离子方程式(总反应)为________________________。
(4)下列实验操作中必要的是____________(填写字母)。
(A)称量电解前的电极的质量;
(B)电解后,电极在烘干称量前,必须用蒸馏水冲洗;
(C)刮下电解后电极上析出的铜,并清洗,称量;
(D)电解后烘干称重的操作中必须按“烘干→称量→再烘干→ 再称量”进行;
(E)在有空气存在的情况下,烘干电极必须用低温烘干的方法。
(5)铜的相对原子质量为_______________________(用带有n、V的计算式表示)。
参考答案:(1)通过消耗H+而调整溶液的pH使之升高,其目的是使Fe3
本题解析:
本题难度:一般
3、选择题 下列关于电解的说法中,正确的是 [???? ]
A.电解池是把化学能转变为电能的装置
B.电解精炼铜时,粗铜板做阴极
C.电镀时,通常把待镀的金属制品做阴极
D.工业电解饱和食盐水用于生产金属钠和氯气
参考答案:C
本题解析:
本题难度:一般
4、实验题 (18分)废旧硬质合金刀具中含碳化钨(WC)、金属钴(Co)及少量杂质铁,利用电解法回收WC和制备CoxOy,的工艺流程简图如下:

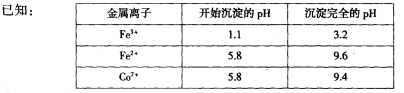
(1)电解时废旧刀具作阳极,不锈钢作阴极,盐酸的作用是______。
(2)通人氨气的目的是调节溶液的pH,除去铁元素。由表中的数据可知,理论上可选择pH最大范围是____________。
(3)实验测得NH4HCO3溶液显碱性,制备CoCO3时,选用的加料方式是_______(填代号),原因是_______。
a.将滤液与NH4HCO3溶液同时加入到反应容器中
b.将滤液缓慢加入到盛有NH4HCO3溶液的反应容器中
c.将NH4HCO3溶液缓慢加入到盛有滤液的反应容器中
写出生成CoCO3的离子方程式______________________________________。
(4)实验中获得的若洗涤不充分,在焙烧时会产生污染性气体,该污染性气体的成分为_______________(填化学式)。
(5)实验室用下列装置制取 ,并测定其化学式。
,并测定其化学式。
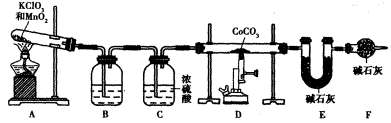
①装置A制得的中含有少量Cl2,则装置B中所盛放的试剂为______(填代号)。
a.NaHCO3溶液??? b.NaOH溶液??? c.KMnO4溶液??? d.饱和NaCI溶液
②在CoCO3完全转化为 后,若称得E管增重4.40g,D管内残留物质的质量是8.30g,则生成物
后,若称得E管增重4.40g,D管内残留物质的质量是8.30g,则生成物 的化学式为____________。
的化学式为____________。
③若缺少装置F,则导致 的值______(填“偏大”、“偏小”或“无影响”)。
的值______(填“偏大”、“偏小”或“无影响”)。
参考答案:(l)作电解质溶液。(2)3.2≤pH<5.8。
(3
本题解析:
试题分析:由题给工艺流程知,以盐酸为电解质溶液,以废旧刀具作阳极,不锈钢作阴极,进行电解,生成WC,溶液中含有亚铁离子和Co2+,加入双氧水,将亚铁离子氧化为铁离子,通入氨气,调节pH在3.2到5.8之间,将铁离子转化为氢氧化铁沉淀过滤除去,滤液中含有Co2+,加入碳酸氢铵溶液生成碳酸钴,焙烧生成CoxOy。(l)电解时废旧刀具作阳极,不锈钢作阴极,盐酸的作用是作电解质溶液。(2)通人氨气的目的是调节溶液的pH,除去铁元素。由表中的数据可知,理论上可选择pH最大范围是3.2≤pH<5.8。(3)实
本题难度:一般
5、选择题 某学生欲完成反应Cu+H2SO4===CuSO4+H2↑而设计了下列四个实验,你认为可行的是
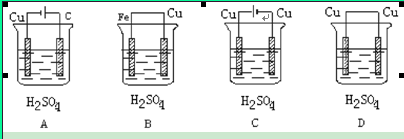
参考答案:C
本题解析:
试题解析:A、该装置为电解装置,铜作阴极,被保护,其实质是电解水,错误;B、该装置是原电池装置,铁作负极,发生氧化反应其方程式为Fe+H2SO4===FeSO4+H2↑,错误;C、为电解装置,阳极铜失电子进入溶液,阴极氢离子得电子生成氢气,正确;D、两极材料相同,不能形成原电池,错误,答案选C。
本题难度:简单