微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 (6分)分别为0.6mol和0.5mol的A、B两种气体,充入0.4L密闭容器中发生反应:3A(g)+B(g) 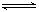 ??mC(g)+2D(g),经5min达到平衡,此时C为0.2mol。又知在此反应时间内D的平均反应速率为0.1mol・L-1・min-1,回答下列问题:
??mC(g)+2D(g),经5min达到平衡,此时C为0.2mol。又知在此反应时间内D的平均反应速率为0.1mol・L-1・min-1,回答下列问题:
(1)m值为?????????????????;
(2)B的转化率为??????????????????????;
(3)平衡时容器内物质的总物质的量为?????????????????????????;
参考答案:(1)2 (2分)(2) 20% (2分)(3)1.1mol
本题解析:(1)D的平均反应速率为0.1mol・L-1・min-1,则生成D是0.1mol・L-1・min-1×0.4L×5min=0.2mol,物质的变化量之比是相应的化学计量数之比,所以m=2。
(2)生成C是0.2mol,则消耗B是0.1mol,所以B的转化率是0.1÷0.5×100%=20%。
(3)由于反应前后体积不变,所以物质的量也是不变的,即还是1.1mol。
本题难度:一般
2、选择题 下列事实不能用勒沙特列原理解释的是(???)
①氯化铁溶液加热蒸干最终得不到氯化铁固体
②铁在潮湿的空气中容易生锈
③把pH=2的NaHSO4溶液加水稀释至10倍,c(OH-)却上升了10倍
④常温下,将1 mL pH=3的醋酸溶液加水稀释至l00 mL,测得其pH<5
⑤在滴有酚酞的Na2CO3溶液中滴CaCl2溶液,生成沉淀的同时溶液颜色由红逐渐变无
⑥对于H2+I2 2HI的平衡体系,加压后密闭体系中的混合气体密度增加
2HI的平衡体系,加压后密闭体系中的混合气体密度增加
⑦在双氧水的分解实验中添加MnO2能使分解速率显著加快
A.①③④
B.②⑥⑦
C.③④⑤
D.②③⑤
参考答案:B
本题解析:
试题分析:勒沙特列原理是化学平衡移动原理,能用该原理解释的事实具备条件是涉及可逆反应平衡移动且符合平衡移动原理。①氯化铁溶液存在平衡:FeCl3+3H2O Fe(OH)3+3HCl,盐类的水解吸热,升高温度平衡正向移动,盐酸易挥发,生成氢氧化铁固体,能用勒沙特列原理解释;②铁在潮湿的空气中能形成原电池,加快腐蚀,不能用勒沙特列原理解释;③NaHSO4溶液加水稀释,涉及水的电离平衡移动,能用勒沙特列原理解释;④常温下,醋酸溶液存在电离平衡:CH3COOH
Fe(OH)3+3HCl,盐类的水解吸热,升高温度平衡正向移动,盐酸易挥发,生成氢氧化铁固体,能用勒沙特列原理解释;②铁在潮湿的空气中能形成原电池,加快腐蚀,不能用勒沙特列原理解释;③NaHSO4溶液加水稀释,涉及水的电离平衡移动,能用勒沙特列原理解释;④常温下,醋酸溶液存在电离平衡:CH3COOH CH3COO-+H+加水稀释,平衡正向移动,能用勒沙特列原理解释;⑤Na2CO3溶液存在CO32-的水解平衡:CO32-+H2O
CH3COO-+H+加水稀释,平衡正向移动,能用勒沙特列原理解释;⑤Na2CO3溶液存在CO32-的水解平衡:CO32-+H2O  ?HCO3-+OH-,加CaCl2溶液,钙离子和碳酸根反应生成碳酸钙沉淀,使平衡向左移动,能用勒沙特列原理解释;⑥对于H2+I2
?HCO3-+OH-,加CaCl2溶液,钙离子和碳酸根反应生成碳酸钙沉淀,使平衡向左移动,能用勒沙特列原理解释;⑥对于H2+I2 2HI的平衡体系,加压,平衡不移动,不能用勒沙特列原理解释;⑦在双氧水的分解实验中加MnO2作催化剂能使分解速率显著加快,不能用勒沙特列原理解释;综上所述选B。
2HI的平衡体系,加压,平衡不移动,不能用勒沙特列原理解释;⑦在双氧水的分解实验中加MnO2作催化剂能使分解速率显著加快,不能用勒沙特列原理解释;综上所述选B。
本题难度:一般
3、选择题 对于可逆反应N2(g)+3H2(g) 2NH3(g)(正反应为放热反应),下列说法中正确的是( )
2NH3(g)(正反应为放热反应),下列说法中正确的是( )
A.达到平衡后加入N2,当重新达到平衡时,NH3的浓度比原平衡的大,N2的浓度比原平衡的小
B.达到平衡后,升高温度,既加快了正、逆反应速率,又提高了NH3的产率
C.达到平衡后,缩小容器体积,既有利于加快正、逆反应速率,又有利用提高氢气的转化率
D.加入催化剂可以缩短达到平衡的时间,是因为正反应速率增大了,而逆反应速率减小了
参考答案:C
本题解析:加入N2,平衡向右移动,NH3的浓度增大,N2的浓度也比原平衡大;升高温度,正、逆反应速率加快,平衡向左移动,NH3的产率减小;缩小容器容积,即增大压强,正、逆反应速率加快,平衡向右移动,H2的转化率提高;加入催化剂能同等程度的加快正、逆反应速率。
本题难度:一般
4、选择题 在一定温度下,反应A2(g)+B2(g) 2AB(g)达到平衡状态的标志是(???)
2AB(g)达到平衡状态的标志是(???)
A.单位时间内生成n mol A2的同时生成n mol AB
B. 容器内的总物质的量不随时间变化
容器内的总物质的量不随时间变化
C.单位时间内生成2n mol AB的同时生成n mol B2
D.容器内A2、B2、AB的物质的量之比是1∶1∶2时的状态
参考答案:C
本题解析:略
本题难度:一般
5、选择题 可逆反应2SO2+O2 2SO3达平衡后,通18O2气体,再次达平衡时,18O存在于(???)
2SO3达平衡后,通18O2气体,再次达平衡时,18O存在于(???)
A.SO3、O2
B.SO2、SO3
C.SO2、SO3、O2
D.SO3、O2
参考答案:C
本题解析:平衡的特征之一是动态平衡,反应可逆,因此,加入18O2后,SO2、SO3、O2中均含有18O。
本题难度:简单