��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪A��BΪ���ʣ�CΪ�������������ת����ϵ

����C����ˮ��õ�ǿ����Һ����A������Na
����C��Һ��Na2CO3��Һ��Ӧ���ų�CO2���壬��A������H2
����C��Һ�еμ�NaOH��Һ�������ɳ��������ܽ⣬��B����ΪAl
����C��Һ�еμ�NaOH��Һ����ɫ�������ɣ���B����Ϊ Cu
��ʵ������ת����ϵ����
A���٢� B���ڢ� C���٢� D���ۢ�
�ο��𰸣�B
���������
�����������2Na+O2 Na2O2��2Na2O2+2H2O=4Na++4OH-+O2����NaOH��Һ������H2��O2��������ת����ϵ������H2+Cl2
Na2O2��2Na2O2+2H2O=4Na++4OH-+O2����NaOH��Һ������H2��O2��������ת����ϵ������H2+Cl2 2HCl��Na2CO3+2HCl=2NaCl+ CO2 �� + H2O��HCl��Һ������H2��Cl2����ȷ����2Al+3Cl2
2HCl��Na2CO3+2HCl=2NaCl+ CO2 �� + H2O��HCl��Һ������H2��Cl2����ȷ����2Al+3Cl2 2AlCl3��AlCl3+3NaOH=Al(OH)3��+3NaCl��Al(OH)3+NaOH=NaAlO2+2H2O��AlCl3��Һ��⣬��������Cl2����������H2������������ת����ϵ������ Cu+Cl2
2AlCl3��AlCl3+3NaOH=Al(OH)3��+3NaCl��Al(OH)3+NaOH=NaAlO2+2H2O��AlCl3��Һ��⣬��������Cl2����������H2������������ת����ϵ������ Cu+Cl2 CuCl2����CuCl2��Һ�м���NaOH��Һ����Cu(OH)2���������CuCl2��������Cu����������Cl2����������ת����ϵ����ȷ��������ʵ������ת����ϵ���Ǣڢܣ�ѡ����B��
CuCl2����CuCl2��Һ�м���NaOH��Һ����Cu(OH)2���������CuCl2��������Cu����������Cl2����������ת����ϵ����ȷ��������ʵ������ת����ϵ���Ǣڢܣ�ѡ����B��
���㣺�������ʵ����ʡ�ת����ϵ��֪ʶ��
�����Ѷȣ�һ��
2������� ij��ѧС������ͼװ�õ��CuCl2��Һ������Ư��Һ��
 ??????
??????
��1���������ķ�Ӧʽ�ǣ�???????????��������W��Ӧ�������?????????���ӡ�
��2��ʵ���������̼���ϳ��˸����к�ɫ���ʣ���������������ɫ���ʡ�
����������ʾ��
�������Ƽ���ѧʽ
| �Ȼ���ͭCuCl
| ��ʽ�Ȼ�ͭCu2( OH)3Cl
|
����
| ��ɫ���塢����ˮ
| ��ɫ���塢����ˮ
?
��ѧС�����������ٺ�ɫ���ʿ�����????????����Cu2O������߶��У��ڰ�ɫ����ΪCuCl
��3��Ϊ̽������̼���ϸ��ŵĺ�ɫ����ɫ���ʣ����������ʵ�飺
ȡ������̼����ϴ�ӡ������������ΪW1g �������������ͼ��ʾװ��b�У�
����ʵ�顣ʵ���У�̼���ϵİ�ɫ������ȫ��Ϊ��ɫ����ˮ����ͭ����ɫ��d�г��ְ�ɫ������ʵ�����ʱ������ͨH2ֱ��̼����ȴ����������ΪW2g ��
��̼���ϵĺ�ɫ������??????????????����ˮ����ͭ��������??????????????????????��
��d�з�Ӧ�����ӷ���ʽ��??????????��
��װ��b�з�����Ӧ�Ļ�ѧ����ʽ��?????????????????????????��
�ܵ��CuCl2��Һʱ�������ϲ�����ɫ���ʵ�ԭ���õ缫��Ӧʽ����Ϊ??????????????????��
�������ϲ�����ɫ���ʵ����ʵ�����?????????����װ��b��ȴʱ������ͨH2�����������Cu+�IJ��ʻ�????????��ƫ��ƫС�����䣩��
�ο��𰸣���1��2Cl- - 2e- = Cl2����? X??��2��C
���������
�����������1���ö��Ե缫���CuCl2��Һʱ������ͬ�ֵ����ų⣬���ֵ���������ԭ���������������ŵ硣���������ӵķŵ�����Cl->OH-.�������ķ�Ӧʽ�ǣ�2Cl- - 2e- = Cl2����XΪ����YΪ������������W��Ӧ�������X���ӣ�������ӦCl2��2NaOH=NaCl��NaClO��H2O������ȡ������Һ��(2)�ٺ�ɫ���ʿ�����Cu; ��3����ʵ���У�̼���ϵİ�ɫ������ȫ��Ϊ��ɫ����ˮ����ͭ����ɫ��֤���ں�ɫ�����в���OԪ�أ�Ҳ�Ͳ���Cu2O��d�г��ְ�ɫ����֤��������AgCl
�����Ѷȣ�����
3������� ��5�֣�����ͼ��ʾ��װ�ý��е�⡣ͨ��һ���������ʪ���KI������ֽ��C�˱�Ϊ��ɫ����
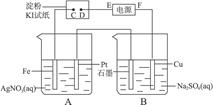
(1)A�з�����Ӧ�Ļ�ѧ����ʽΪ_________________________________��
(2)��B�й۲쵽��������__________________________��______________________��______________________��
(3)�����£����ӵ�ʼ��ʱ��t sʱ��A��Bװ���й��ռ�����״���µ�����0.168 L����������������������Ӧ���������ⶨ����A����Һ���ǡΪ1000 mL����A��Һ��pHΪ______________________��
�ο��𰸣�(1)4AgNO3+2H2O �����������1�����������Ϊ��·�д�����3�����ء���ѡ��һ��Ϊ�о�����ʱ�������2���ɿ�������·����衣 �����������1�����������Ϊ��·�д�����3�����ء���ѡ��һ��Ϊ�о�����ʱ�������2���ɿ�������·����衣

��ѡ��ʪ���KI������ֽΪ�о���������C�˱�Ϊ��ɫ����֪C����I2���ɣ�2I--2e-====I2��
I2ʹ���۱���ɫ���÷�Ӧ���ڵ��ص����������ķ�Ӧ���ɴ˿��Զ϶���ӵ�Դ��E��Ϊ������F
�����Ѷȣ���
4��ѡ���� LiFePO4��������Ӷ������������ص����Ƴ�Ϊ���˻���ɫ��Դ���³衣��֪�õ�طŵ�ʱ�ĵ缫��ӦʽΪ������ FePO4+Li++e-==LiFePO4 ���� Li��e-==Li+����˵������ȷ���� [???? ]
A�����ʱ��ط�ӦΪFePO4+Li=LiFePO4
B�����ʱ��������ϱ�ע��+���ĵ缫Ӧ����ӵ�Դ����������
C���ŵ�ʱ����ڲ�Li+���ƶ�
D���ŵ�ʱ������������Li+�õ��ӱ���ԭ
�ο��𰸣�B
���������
�����Ѷȣ�һ��
5������� �Ե绯ѧ�����ϳ��л����Ϊ�л���ϳɡ��л���ϳ���һ���л���ѧ���绯ѧ�ͻ�ѧ���̶�ѧ�������Ŀ�ѧ���ǵ绯ѧ���л��ﻯ�������е���ҪӦ�á�������л���ϳɱ���Ϊ�����ϵķ�����ո�µļ��������л���ϳɵ��о��Ѿ�����170������������ʷ������1834�꣬Ӣ����ѧ��Faraday�õ���������Һ�Ƶ����飬����˵����ʵ����������ʵ�ֵ��л���ϳɡ� 2CH3COO-?-?2e-?=?C2H6��+?2CO2��??(a)
��1��������Ӧ(a)������________������ء���ԭ��ء�?����________����
��2�������л������ض���װ���ڽ���������ͬʱ���ɲ������ܣ�����װ�ü�Ϊȼ�ϵ�ء����磬��ϩ������������ȩ�Ļ�ѧ��Ӧ��2CH2=CH2?+?O2��2CH3CHO����Ƴ�ȼ�ϵ�أ�������CH2=CH2+H2O�C2e-=CH3CHO+2H+??????������______________________��ع���ʱ������������Һ��pH____________������ߡ��������͡����䡱����?
��3��ȼ�ϵ�����ھ�������ת��Ч�ʸߡ��Ի�����ȾС���ŵ���ܵ�����������ձ����ӡ�

�ٸ��ݱ��������ݿ��Կ�����__________��ɵ���Ⱦ��Ϊ���أ�����Ļ���������Ҫ��__________�����ꡣ
A��ˮ��????B�������㱻�ƻ�????C���⻯ѧ����????D����ϫ????E����ɫ��Ⱦ
�����ҹ������������Ҫ����ΪSO2����SO2���մ����ķ����ܶ࣬����һ���ǽ�SO2ͨ��ʯ����[Ca(OH)2]�У����Ƶ�ʯ��[CaSO4��2H2O]����д����Ӧ�Ļ�ѧ���̣�_________________________��CaSO4?+?2H2O?=?CaSO4��2H2O��
�ο��𰸣���1�����أ�����
��2��1/2O2+2H++2e-=
���������
�����Ѷȣ�һ��
|