微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 如下图所示,可形成氢氧燃料电池。通常氢氧燃料电池有酸式(当电解质溶液为硫酸时)和碱式〔当电解质溶液为NaOH(aq)或KOH(aq)时〕两种。试回答下列问题:
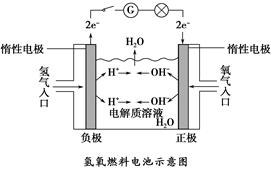
(1)酸式电池的电极反应:负极_______________,正极______________;电池总反应:________________;
电解质溶液pH的变化________(填“变大”“变小”或“不变”)。
(2)碱式电池的电极反应:负极_________________,正极_________________;电池总反应:______________;电解质溶液pH的变化________(填“变大”“变小”或“不变”)。
参考答案:(1)2H2-4e-=4H+ O2+4e-+4H+=2H2O
本题解析:(1)正极上,O2得电子变为O2-,溶液中O2-不能单独存在;酸性条件下与H+结合生成H2O。负极上,H2失电子变为H+,H+进入电解质溶液。电池总反应为H2和O2生成水的反应,由于有水生成,溶液将逐渐变稀,故pH增大。
(2)正极上,O2得电子变为O2-,溶液中O2-不能单独存在,碱性条件下与H2O分子结合生成OH-;负极上,H2失去电子变为H+,碱性条件下H+不能大量存在,与OH-结合生成水。电池总反应也是H2和O2生成水的反应。同样,由于有水生成,c(OH-)变小,pH变小。
本题难度:一般
2、选择题 下列反应不可能是原电池反应的是
A.Fe + 2H+ = Fe2+ + H2↑
B.H+ + OH- = H2O
C.2H2 + O2 = 2H2O
D.Fe2+ + Zn =" Fe" + Cu2+
参考答案:B
本题解析:
试题分析:只有自发的、放热的氧化还原反应才能设计成原电池,酸碱中和反应是复分解反应,非氧化还原反应,不可能是原电池,选B。
考点:考查原电池的构成条件。
本题难度:一般
3、选择题 2013年12月31日夜,上海外滩运用LED产品进行了精彩纷呈的跨年灯光秀。下图是一种氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是???
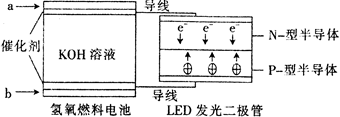
A.a处通入氧气
B.b处为电池正极,发生了还原反应
C.该装置中只涉及两种形式的能量转化
D.P-型半导体连接的是电池负极
参考答案:B
本题解析:
试题分析:由于电子从在LED发光二极管的N极向P极移动,所以N极与电源的负极连接,P极与电源的正极连接。所以在燃料电池中a处通入的气体为氢气,该处为负极,发生氧化反应;在b处通入的气体为氧气,该处为正极,发生还原反应。在该装置中涉及的能量转化形式有化学能转化为电能,以及电能转化为光能及热能。所以正确选项为B。
本题难度:一般
4、选择题 混合动力车的电动机目前一般使用的是镍氢电池,在上坡或加速时,电池处于放电状态,
在刹车或下坡时电池处于充电状态.镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解液.镍氢电池充放电原理如图,其总反应式为:
??H2+2NiOOH

?2Ni(OH)2
下列有关混合动力车的判断正确的是( )
A.在上坡或加速时,乙电极周围溶液的pH将减小
B.在刹车和下坡时,乙电极增重
C.在上坡或加速时,溶液中的K+向甲电极迁移
D.在刹车和下坡时,甲电极的电极反应式为2H2O+2e-=H2↑+2OH-

参考答案:A、混合动力车上坡或加速时,属于原电池的工作原理,电动机提供
本题解析:
本题难度:简单
5、填空题 右下图是以Zn和Cu为电极,稀硫酸为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
实验后的记录:
①Zn极发生还原反应,Cu极发生氧化反应
②H+向负极移动
③电子流动方向Zn→导线→Cu
④溶液的pH变小
⑤若有1mol电子流过导线,则产生H2为0.5mol。
⑥正极的电极反应式:Zn-2e- =Zn2+
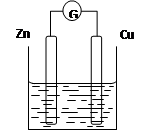
(1)在卡片上,叙述合理的是___ ????__(填序号)。
(2)其他条件相同情况下,产生气泡的速率比单一锌片??????(填快或慢)。
(3)在实验中,甲同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是___________________________。
(4)如果把硫酸换成硫酸铜溶液,猜测___(填“锌极”或“铜极”)变粗,原因是____?__(用电极方程式表示)。实验结束后称得两极质量差12.9g,假设初始时Zn极与Cu极质量相等,则反应中转移的电子的物质的量为?????mol。
参考答案:(1)3、5(2)快(3)锌片中含有杂质(4)铜极、Cu2+
本题解析:
试题分析:(1)原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。锌比铜活泼,所以锌是负极,失去电子。铜是正极,溶液中的氢离子在正极得到电子,发生还原反应生成氢气。据此可知选项③⑤正确。
(2)通过原电池进行的反应速率快。
(3)由于锌片中含有杂质,从而也构成原电池,故锌片表面也有气泡产生。
(4)如果把硫酸换成硫酸铜溶液,则正极是铜离子放电生成单质铜,所以铜极变粗。电极反应式是Cu2++2e-=C
本题难度:一般
|