微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知外电路中,电子由铜流向a极。有关下图所示的装置分析合理一项是(???)
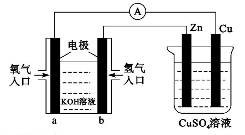
A.该装置中Cu极为正极
B.当铜极的质量变化为12.8 g时,a极上消耗的O2在标准状况下的体积为2.24 L
C.b极反应的电极反应式为:H2一2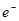 = 2H+
= 2H+
D.一段时间后锌片质量减少
参考答案:B
本题解析:
试题分析:外电路中,电子由铜流向a极,故铜为负极,A错误;a极为正极,b极为负极,锌为正极;当铜极的质量变化为12.8 g时,即有0.2mol的铜溶解,转移0.4mol电子,故a极上消耗的O2在标准状况下的体积为2.24 L,B正确;b极为负极,氢气发生氧化反应,但是该电解质为碱性溶液,氧化产物不可能是氢离子,而是水,C错误;锌片是正极,质量不会减少,表面还会附着铜,D错误。
点评:原电池是历年高考常考知识点,注重考查学生分析问题、解决问题的能力。
本题难度:一般
2、填空题
中国是世界上最早研究和生产合金的国家之一。
①在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其成分金属的熔点____________。
②现有A、食盐???B、石英?C、干冰三种晶体,请比较三者的熔点高低,按照从高到低的顺序排列___________。(用序号表示)铜器表面容易生成一层薄薄的铜绿[主要成份是Cu2(OH)2CO3],请写出铜在潮湿的空气发生电化学腐蚀时的负极反应式____________?;用盐酸可以除去铜器表面的铜绿,该反应的化学方程式为______________。
③下列对金属制品采取的防护方法不正确的是____________(填序号)。
A.在电线的外面包上一层塑料层??????
B.在自行车钢圈上镀上一层金属铬? C.在海轮的铁制外壳上焊上铜块
参考答案:①低??
②?B?>?A?>?C??;Cu
本题解析:
本题难度:一般
3、选择题 在钢铁腐蚀过程中,下列五种变化可能发生的是( )
①Fe由+2价转为+3价???
②O2被还原、
③产生H2、
④Fe(OH)3失水形成Fe2O3-xH2O、
⑤杂质碳被氧化.
A.①②③④
B.只②③④
C.只①②
D.①②③④⑤
参考答案:钢铁生锈的过程是金属铁发生了吸氧腐蚀(或是析氢腐蚀)的原电池
本题解析:
本题难度:一般
4、选择题 钢铁腐蚀在生活和生产中相当普遍.下列措施能防止钢铁腐蚀的是( )
A.把钢铁雕塑焊接在铜质基座上
B.将输送自来水的铁管表面镀锌
C.经常用自来水冲洗钢铁制品
D.将输油铸铁管道埋在潮湿、疏松的土壤中
参考答案:A、把钢铁雕塑焊接在铜质基座上,则金属铁做原电池的负极,会加
本题解析:
本题难度:简单
5、填空题 下图两个装置中用滴有酚酞的NaCl溶液做电解质溶液,进行化学能和电能相互转化的研究。请回答:
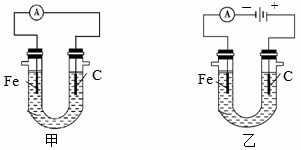
(1)写出两个铁电极上的电极反应式。
甲:??????????????????????????????
乙:??????????????????????????????
(2)甲装置中????电极附近的溶液先变红,乙装置中???电极附近的溶液先变红。
(3)检验乙中C电极反应产物的方法是?????????????????????????。
(4)电解氯化钠稀溶液可制备“84消毒液”,通电时氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出相应的化学方程式:????????????????????????????????。所得消毒液中离子浓度的由大到小顺序????????????????????????????????。
(5)如果起始时乙中盛有足量一定浓度的CuSO4溶液,反应一段时间后,要使溶液恢复到以前的状态,可向溶液中加入一定量的????????????(填化学式)。
参考答案:(14分)(1)Fe ―2e- = Fe2+????????
本题解析:
试题分析:(1)根据装置的特点可知,甲是原电池,铁是负极,发生吸氧腐蚀,负极电极反应式是Fe-2e-=Fe2+。乙是电解池,铁电极和电源的负极相连,作阴极,电极反应式是2H+ + 2e-= H2↑。
(2)甲装置中碳棒是正极,氧气得到电子,生成OH-,所以碳棒电极附近的溶液先变红;乙装置中铁电极是阴极,溶液中的氢离子放电,破坏了阴极周围水的电离平衡,所以阴极周围溶液显碱性,所以铁电极附近的溶液先变红。
(3)乙中C电极反应产物是氯气,具有强氧化性,所以检验的方法是用湿润的淀粉碘化钾试纸
本题难度:一般