微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
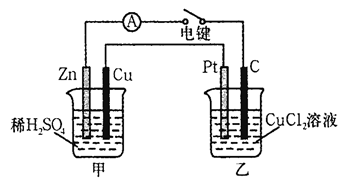
1、填空题 (Ⅰ)某兴趣小组的同学用下图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流计的指针发生了偏转。请回答下列问题:
 ?
?
(1)甲装置的名称是____________ (填“原电池”或“电解池”)。
(2) 写出电极反应式: Pt极????????????????????????????????; 当甲中产生0.1 mol气体时,乙中析出铜的质量应为______________。
(3)若乙中溶液不变,将其电极都换成铜电极,电键闭合一段时间后,乙中溶液的颜色___________(填“变深”、“变浅”或“无变化”)。
(Ⅱ)燃料电池是燃料(如CO、H2、CH4等)跟O2(或空气)反应,将化学能转化为电能的装置。对于以强碱为电解质的CH4燃料电池,负极电极反应式为:??????????????????????????????????????,随着放电的进行,溶液的pH????????????(填“变大”“变小”或“不变”)。
(Ⅲ)由Cu2+、Cl-、Na+、SO42-四种离子中的两种离子组成的电解质溶液若干种,可选用铜电极、铂电极进行电解实验。
(1)要使电解过程中溶质的组成和质量不变,而该稀溶液的浓度增大,又无浑浊,应以?????_______为阳极电解??????????溶液,阳极电极反应式为 ????????????????????????。
(2)以铂作阳极电解????????????溶液时,溶液的碱性有明显增强,且溶液保澄清,电解的总反应式为?????????????????????????????????????????????????????。
参考答案:(Ⅰ)(1)原电池?(1分)?(2)2Cl- - 2e-=
本题解析:
试题分析:(Ⅰ)(1)由图中的铜、锌两种电极和电解质稀硫酸和闭合电路可判断:该装置为原电池,Zn比铜活泼,则Zn作负极,Cu作正极,发生电池反应为Zn+H2SO4=ZnSO4+H2↑,电子由负极流向正极,该装置将化学能转变为电能,即甲装置的名称是原电池。
(2)甲装置为原电池,将化学能转变为电能,乙装置为电解池,石墨和铂都为惰性电极,连接电源正极的铂电极为电解池的阳极,溶液中的氯离子放电,发生氧化反应:2Cl--2e-=Cl2↑。连接电源负极的碳电极为电解池的阴极,溶液中的铜离子放电,发生还
本题难度:一般
2、选择题 下列金属防腐措施中,利用原电池原理的是( )
A.在金属表面喷漆
B.在金属中加入一些铬或镍制成合金
C.在轮船的壳体水线以下部分装上锌块
D.使金属表面生成致密稳定的氧化物保护膜
参考答案:A、在金属表面喷漆,只是阻止了金属和电解质溶液接触,不能构成
本题解析:
本题难度:简单
3、填空题 (10分)钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程中的有关问题。
(1)下列哪个装置可防止铁棒被腐蚀_____________ 。
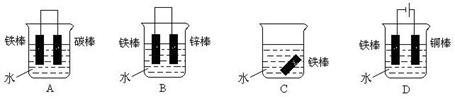
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如右: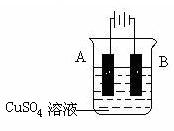
请回答:
①A电极对应的金属是______(写元素名称),B电极的电极反应式是????????????。
②若电镀前铁、铜两电极的质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为51.2 g,则电镀时电路中通过的电子物质的量为_______。
参考答案:(1)BD(2分)?(2)①铜(2分)?? Cu2+ +2e
本题解析:略
本题难度:简单
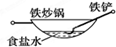
4、选择题 相同材质的铁在下图中的四种情况下最不易被腐蚀的是 ( )
 ?
? ?
?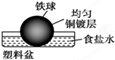 ?
?
A??????????????????? B??????????????? C????????????????????? D
参考答案:C
本题解析:
试题分析:A、铁做负极、铜做正极,食醋为电解质溶液,形成原电池,铁发生电化学腐蚀,故A不选;B、铁做负极、合金中的碳等材料做正极,食盐水为电解质溶液,形成原电池,铁发生电化学腐蚀,故B不选;C、铁被均匀的铜镀层保护,不易被腐蚀,故C正确;D、铁做负极、铜做正极,酸雨为电解质溶液,形成原电池,铁发生电化学腐蚀,故D不选,故选C。
本题难度:一般
5、选择题 下列说法正确的是[???? ]
A.铅蓄电池放电时铅电极发生还原反应
B.电解饱和食盐水在阳极得到氯气,阴极得到金属钠
C.给铁钉镀铜可采用CuSO4作电镀液
D.生铁浸泡在食盐水中发生析氢腐蚀
参考答案:C
本题解析:
本题难度:一般