微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 为制备干燥、纯净的CO2,将大理石和盐酸反应生成的气体先后通过装有下列物质的两个吸收装置,两个装置中应依次装入
A.饱和Na2CO3溶液;无水CaCl2固体
B.饱和NaHCO3溶液;浓H2SO4
C.浓H2SO4;饱和Na2CO3溶液
D.饱和Na2CO3溶液;稀H2SO4
参考答案:B
本题解析:
试题分析:盐酸易挥发,所以生成的CO2中除了含有水蒸气以外,还有氯化氢气体。首先要除去氯化氢,利用饱和的碳酸氢钠溶液,最后通过浓硫酸干燥即可,答案选B。2制备中除杂的有关判断
点评:该题是基础性试题的考查,试题注重基础,侧重对学生基础知识的巩固与训练,难度不大,有助于培养学生规范、严谨的实验设计能力,提升学生的学科素养。
本题难度:简单
2、选择题 用0.20mol/L的NaOH溶液滴定100.0mL0.20mol/LHCl溶液时,滴定误差在±0.1%以内,反应完毕后溶液的pH变化范围是
A.5~9
B.4.0~10.0
C.4.3~9.7
D.以上都不正确
参考答案:B
本题解析:
试题分析:(1)计量点前计量点前误差为+0.1%时,即滴入NaOH的体积为99.9mL,NaOH不足。
此时锥形瓶溶液中是中和生成的NaCl和剩余的HCl。所以只要计算该溶液的PH值即可。
剩余的n(HCl)=n(HCl总)-n(NaOH)=0.2*(100.00-99.9)*10^-3=2*10^-6(mol)
则PH(前)=lg[c(HCl)]=4。
(2)计量点后半滴,即加入NaOH的体积为100.1mL,NaOH过量,此时为NaCl和NaOH的混合溶液,所以计算时只需考虑NaOH即可。
n(NaOH过量)=n(NaOH总)-n(NaOH反应)=0.2*(100.1-100)*10^-3)=2*10^-5(mol)
此时溶液体积v=100.00+100.1=200.1mL=200.1*10^-3(L),
所以[OH-]=n(NaOH过量)/v="2*10^-5/(200.1*10^-3)=1/100.05" *10^-2(mol/L)
[H+]=10^-14/[OH-]? PH(后)=-lg[H+]=10所以突跃范围为4~10。故选B。
点评:酸碱中和滴定突跃范围的计算实际上也是强酸、强碱互相混合的计算,其规律是
(3)酸I+碱II
完全中和:[H+] =" [OH-]" = 1 mol/L
mol/L
酸过量:? [H+]= 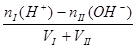
碱过量:[OH-] = 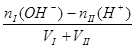
滴定突跃范围指计量点前半滴和后半滴滴定剂所引起的锥形瓶中溶液PH值的变化范围。要控制误差为+/-0.1%时。由于计量点时酸碱恰好完全反应,也就是滴入NaOH的体积为100.00mL时达计量点,所以计量点前误差为+0.1%时,是指加入NaOH的体积为99.9mL,而计量点后误差为-0.1%时指加入NaOH的体积为100.1mL。因此计算滴定突跃范围,只要计算出计量点前、后半滴时锥形瓶中溶液的PH(前)和PH(后)即可。
本题难度:简单
3、填空题 实验室制取下列气体时,应选用下列哪种酸:(填入相应的字母。)
A.浓盐酸
B.稀盐酸
C.稀硫酸
D.浓硫酸
⑴用大理石和?????????制CO2 ;?⑵用MnO2和???????????制Cl2;
⑶用锌粒和???????????????制H2 ;??⑷用食盐和????????????????制HCl。
参考答案:(1) B?? (2) A?? (3) B或C? (4) D
本题解析:略
本题难度:简单
4、选择题 某无色气体可能由 O2、 CO2、 HCl、NH3、NO 、 Br2??中的一种或几种组成 , 通过图中洗气瓶后气体体积减少 , 通过干燥管后气体呈红棕色 , 则下列推断正确的是:
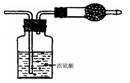
A.干燥管内固体为碱石灰
B.原气体中一定有 NO 和 O2
C.原气体中一定有NH3、NO 、CO2
D.原气体中有 HC1、 Br2
参考答案:C
本题解析:略
本题难度:简单
5、计算题 (6分)某学生准备用质量分数为37%、密度为1.19 g・cm-3的浓盐酸配制0.10 mol・L-1的稀盐酸500 mL。请完成下列问题:
(1)量取浓盐酸的体积为_________ mL,应选用量筒的规格为_________ mL。
(2)配制时应选用容量瓶的规格为_________ mL。
(3)需用的仪器有:容量瓶、___________、___________、___________和试剂瓶等。
参考答案:(1)4.1? 5或10
(2)500
(3)烧
本题解析:根据所配制稀盐酸的物质的量的浓度和体积可以算出溶质的物质的量,再根据溶质的物质的量和质量分数可以求出溶液的质量,根据溶液的质量和密度可以求出量取浓盐酸的体积;量筒的规格选用应该遵循与溶液体积接近的原则;根据所配制稀盐酸的体积可以选用容量瓶的规格;根据配制的各步骤可以确定需用的仪器。
本题难度:简单